
2021-09-30 10:57:31來源:藥智網瀏覽量:432
導讀:金娃娃?
美東時間9月27日晚,華爾街日報透露:默沙東即將達成以110億美元收購制藥公司Acceleron,而這一金額也將成為默沙東歷史上自411億美元收購先靈葆雅之后最大一筆收購交易。
Acceleron是一家臨床階段的生物制藥公司,專注于抗癌藥和針對罕見病的孤兒藥的研發,目前管線上的產品主要針對呼吸系統和血液學。
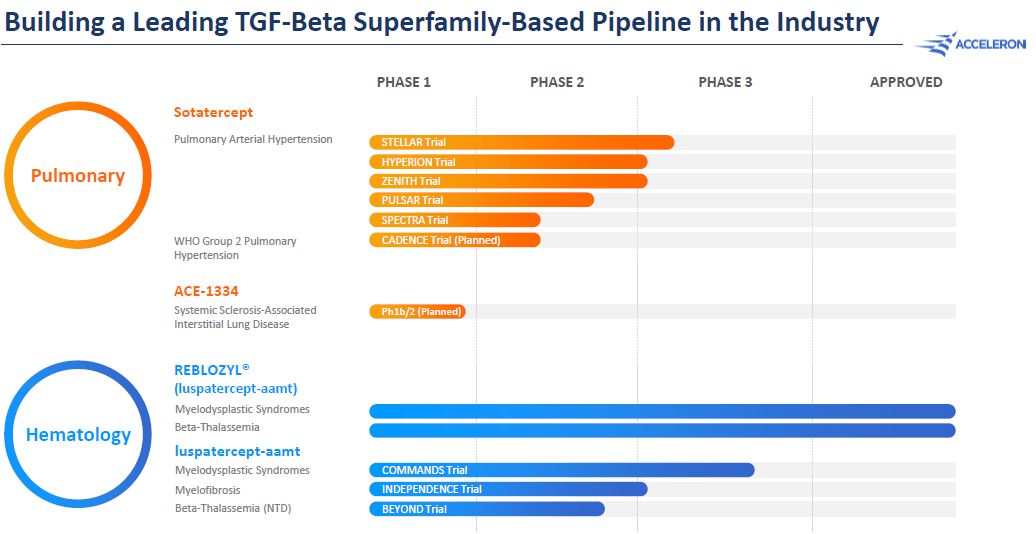
圖1Acceleron的研發管線
面臨K藥的專利懸崖,默沙東選擇了布局罕見病領域,押注了下一個“金娃娃”的未來。
針對罕見病領域治療的孤兒藥,到底有什么魅力?
孤兒藥,3833億藍海
提到罕見病和孤兒藥,許多人會覺得其市場并不大,其實并不然。
據Frost&Sullivan資料顯示,全球罕見病藥物市場規模將由2020年1351億美元增至2030年3833億美元,年復合增長率達11%。
其中,由于近年來我國在政策等多方面開始推進罕見病藥物的創新發展,預計中國罕見病藥物市場將由2020年13億美元急速增長至2030年259億美元,年復合增長率高達34.5%。
表1 按地區劃分的全球罕見病藥物市場規模增速(預測)
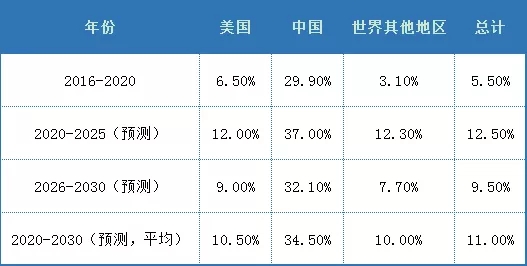
孤兒藥全球市場潛力巨大,回報極其誘人。
截至2020年末,FDA已授予5712個孤兒藥資格,批準930個孤兒藥適應癥。
據不完全統計,僅美國FDA批準孤兒藥上市達到592個(按適應癥計),光2020年批準的53款創新藥中,有31款,占據58%比例的藥物,都被批準用于治療罕見病或孤兒病。
另外,2020年全球十大暢銷孤兒藥合計銷售額達到428億美元,其中四種治療腫瘤適應癥,其余六種針對需要接受長期治療的罕見病。
十大孤兒藥中Ocrevus、Darzalex、Soliris屬于化學藥物,其余七中為生物制藥。
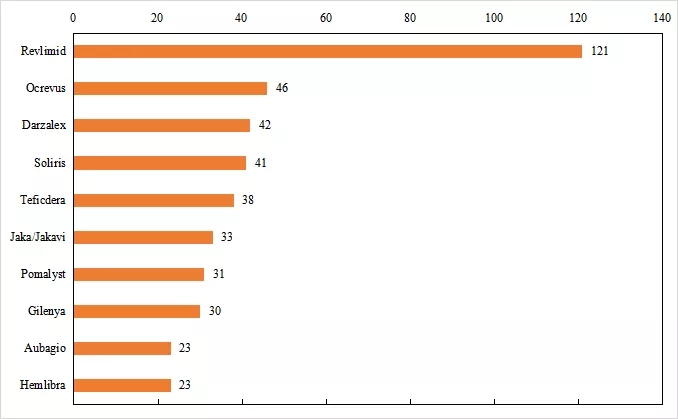
圖2 2020年全球孤兒藥品牌銷售額Top10
銷售額:億美元
當前,全球孤兒藥市場幾乎被諾華、羅氏、新基等國際制藥巨頭占據。
根據醫藥咨詢公司IgeaHub報告,Top10企業占據了孤兒藥市場的54.9%。
其中,諾華在孤兒藥市場中相對領先,占據11.3%的市場份額;緊隨其后的是羅氏和新基,各占據8.8%和8.0%的市場份額;
之后是百時美施貴寶(5.8%)、夏爾(4.7%)、輝瑞(4.6%)、賽諾菲(3.2%)、拜耳(3.1%)、Alexion(2.7%)和百進(2.7%)。
在2020年全球孤兒藥品牌銷售額Top10品種中,諾華、羅氏各下2城,新基、百時美施貴寶、賽諾菲、Alexion等各占1城。
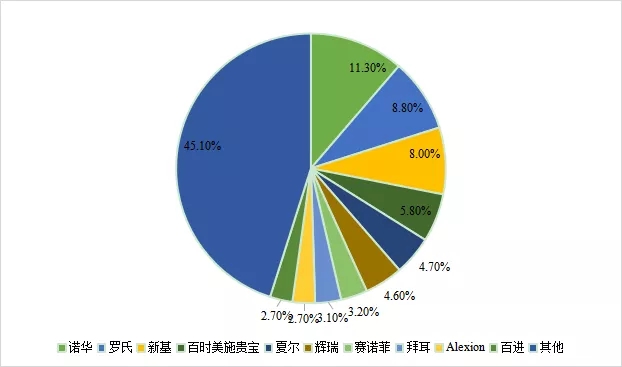
圖3 全球孤兒藥市場份額企業分析
以目前全球已發現的罕見病及藥物上市比例測算,中國目前還存在巨大的缺口。
全世界已經發現的罕見病在7000種左右,80%為遺傳性疾病,罕見病患者中兒童約占一半,1歲以下嬰兒死亡原因中,約35%是由罕見病引起的。
而中國已上市罕見病相關藥物70余種,涉及60余種罕見病。
不到1%的罕見病有上市藥物可供使用治療,超過99%的罕見病束手無策,孤兒藥領域處于空白。
孤兒藥研發難點在哪?
盡管近年來我國孤兒藥政策鼓勵逐漸增多,但是孤兒藥研發難度遠超過普通新藥的局面并未發生根本性改變。
孤兒藥研發總體有以下三大障礙:
1、臨床試驗難度極大
罕見病單一病種受眾少、治療難度大,孤兒藥在研發過程中需要滿足新藥研發基本的臨床要求,但是,受眾數量少這一典型特征就難以滿足新藥研發臨床試驗的要求,大大延長了新藥研發的周期和招募費用。
此外,多數罕見病是遺傳病,超過50%會發生于兒童階段,臨床試驗在道德和法律上都存在著風險。
2、市場機制失靈
前端研發成本高昂,而后端孤兒藥市場又缺乏保障,在某種程度上,孤兒藥市場屬于一個“不完善市場”,存在著高度市場失靈性。
對比于普通的新藥研發,孤兒藥更高風險、更高成本、更長周期,而帶來的不一定是更大的回報,讓眾多觀望的藥企望而卻步,進一步陷入死循環。
如果政府不加干涉,僅由市場調節,那藥企的積極性會進一步喪失,罕見病患者將作為市場失靈的直接受害者,無藥可醫。
另外,孤兒藥具有高度的信息不對稱性,我國尚未形成罕見病和孤兒藥的大數據平臺,特別是在偏遠地區,由于通信設施和醫療條件落后,存在無法確診和確診后無法治療跟蹤的情況,藥企更難以把握孤兒藥的供應方向。
更少的經驗和案例,進一步增加了研發的不確定性。
3、孤兒藥使用配套的醫保報銷制度滯后
我國孤兒藥長期依賴進口,藥價高昂,及時有藥可醫,大部分家庭都是難以承擔的。
藥價擋在患者和藥企之間,這只攔路虎阻礙了中國孤兒藥市場的發展。
僅是公共福利性質的公共產品,就決定了只有個別嚴重程度更大的罕見病患者可以獲得救濟,另外將近7000種罕見病患者的用藥,則只能“望天興嘆”。
孤兒藥的可得性和可負擔性,建立提高基層醫生對罕見病的識別能力等,都是需要深入考慮和關注的問題。
實現罕見病藥品可及性,對策有哪些?
目前,我國正在努力填補罕見病領域的空白,引領更多醫藥企業進軍該市場。
在全球孤兒藥市場逐年擴增之際,我國如何加速孤兒藥研發及上市?
有以下對策考量:
1、建立罕見病藥品的信息制度,增強其可獲得性
罕見病藥品信息對于實現罕用藥可及性具有重要意義,應建立多方主體參與、信息實時共享、公開透明的罕見病藥品信息平臺。
政府部門主導建立信息平臺和反饋平臺,藥品生產流通企業在進行生產經營活動時也須承擔部分社會責任,醫療機構在診治中,對罕見病進行收集整理上報。這樣才可能更全面掌握罕見病總體情況,并作出制度性安排。
2、完善藥品保障制度,促進罕用藥的可供應性
追求利益最大化是企業的核心目標,因此藥品成本高、利潤低造成生產商積極性低是藥品短缺的重要原因之一。
在前期階段,政府應設立專項研發費用基金,加大研發費用的扶持。
在準入引進環節,政府需完善罕用藥的審批制度,結合罕見病的特殊性適當調整審核標準以加快審批速度。
在上市后階段,給予罕見病藥品企業一定的稅收優惠及一定年限的藥品壟斷權,通過政策傾斜減少其后顧之憂提高生產積極性。
3、完善醫療保障制度,提高患者可負擔性
逐步將罕見病納入社會基本醫療保險,且將部分治療效果優良的罕用藥納入國家基本藥物目錄。
為保證權利的一致性,政府應通過立法規定商業保險不可為追求利益而拒絕罕見病患者投保,政府可和保險公司商討專門的罕見病保險種類,包括罕見病種類及報銷比例等。
對于進口依賴程度高的罕用藥,政府作為民眾利益代表者應利用信息平臺,充分獲取國內罕用藥需求,加大與國外企業談判力度,以更優惠的價格引進藥品,以權威渠道來保障進口罕用藥的質量、價格及供應。
愿藥企同道們一起努力,讓孤兒藥成為企業愿意押注的未來,讓罕見病患者能夠觸手可及孤兒藥。
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容!