
2021-07-14 15:02:56來源:新浪醫藥瀏覽量:410
導讀:從Nature預測的前列腺癌藥物市場看,整體前列腺癌藥物市場體量會增大近2倍,將在2029年達到300億美元。
前列腺癌是一種男性雄激素依賴的腫瘤,轉移性前列腺癌患者常用藥物去勢治療(ADT),最初應答率能達80-90%,但幾乎所有患者最終都在去勢治療后進展為轉移性去勢抵抗性前列腺癌(mCRPC),這類患者5年生存率僅為30%。
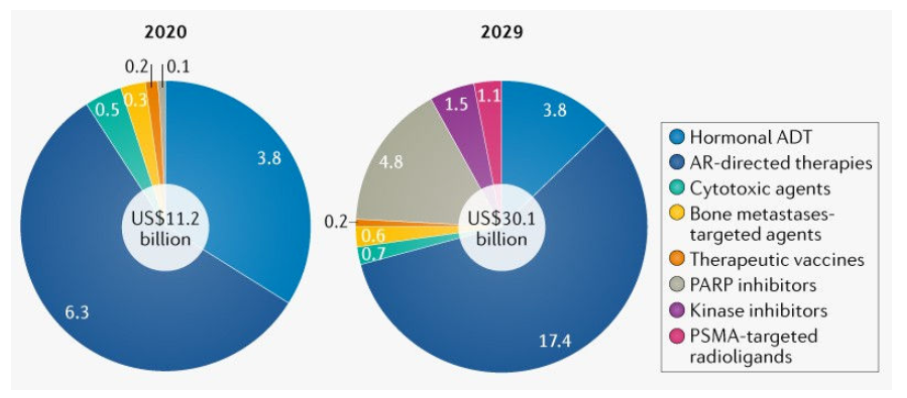
圖1 前列腺癌藥物治療市場變化
從Nature預測的前列腺癌藥物市場看,整體前列腺癌藥物市場體量會增大近2倍,將在2029年達到300億美元,這其中傳統去勢治療ADT使用將減少,以重磅炸彈藥物Zytiga(醋酸阿比特龍)和Xtandi(恩雜魯胺)為主的雄激素受體(AR)拮抗劑顛覆了轉移性前列腺癌的治療格局,市場占有量將繼續增大,PARP抑制劑和PSMA放射配體療法爭得一席之地的機會,包括Akt抑制劑在內的激酶抑制劑也會對細分人群起作用。
AR拮抗劑引領市場擴大
強生的Zytiga和安斯泰來/輝瑞的Xtandi分別于2011和2012年獲FDA批準上市,同為AR拮抗劑,但前者通過抑制CYP17而減少雄激素的生物合成,后者則是阻止雄激素受體轉運至細胞核。
強生通過上市兩個AR拮抗劑藥物而占據轉移性前列腺癌霸主地位。一個是阿比特龍,另一個是在2013年從Aragon制藥買來的阿帕魯胺,是FDA首個批準的用于非轉移性去勢抵抗性前列腺癌的藥物,在此之前,ADT治療后前列腺特異性抗原(PSA)升高但無轉移的CRPC患者無標準治療選擇。今年又通過腫瘤實時審評計劃,批準用于與ADT聯用于轉移性去勢敏感性前列腺癌,會成為后阿比特龍時代的主力軍。
表1 FDA上市的四個第二代抗雄激素藥物
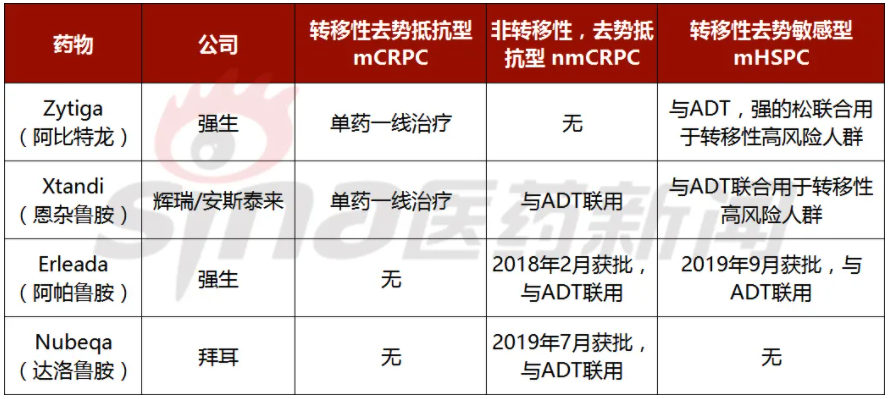
恩雜魯胺將現在是FDA批準的第一種也是唯一一種口服治療三種不同類型的晚期前列腺癌——非轉移性和轉移性去勢抵抗性前列腺癌(CRPC)和mCSPC。將安斯泰來和輝瑞都帶入前列腺癌治療領域第一梯隊。
當年安斯泰來花了7.65億美元從Medivation(后被輝瑞收購)買到Xtandi(恩雜魯胺)除美國外的商業權益,同時美國的銷售額平分。安斯泰來在泌尿生殖方面有市場基礎,分別在2004和2012年,先后在歐洲和日本上市了第一代抗雄激素藥物,Eligard(醋酸亮丙瑞林)和Gonax(地加瑞克),還上市了幾個產品也為泌尿生殖系統藥物。輝瑞幾乎擁有了小分子抗癌藥全明星陣容——用于前列腺癌的恩雜魯胺,和當年收購Medivation獲得的他拉唑帕尼。
拜耳終于在上市針對前列腺癌骨轉移的Xofigo(鐳-223)6年后進入主要治療市場。達洛魯胺相對于之前上市的二代抗雄激素藥物主要優勢是減少可能的不良反應,透過血腦屏障低能減少CNS相關不良反應。
PARP抑制劑加入前列腺癌競爭
目前PARP抑制劑在前列腺癌市場沒有在卵巢癌中競爭那么激烈。在2020年,兩個PARP抑制劑首先被FDA批準用于AR拮抗劑經治后的mCRPC,分別是奧拉帕利和盧卡帕尼,前者用于治療攜帶同源重組修復(HRR)基因改變的患者,約占20-30%的mCRPC人群,后者用于紫杉類方案化療后進展并攜帶DDR基因缺陷(BRCA1/2)的患者,約占12%的mCRPC人群。從人群上來看,盧卡帕尼略受限制。
奧拉帕利是阿斯利康近10多年來前列腺癌領域批準的第一個新藥,曾在20世紀90年代上市了兩個第一代雄激素受體抑制劑,Zoladex(戈舍瑞林)和Casodex(比卡魯胺)。與默沙東合作開發的PARP抑制劑Lynparza(奧拉帕利),是至今獲批適應癥最多的PARP抑制劑,適應癥涵蓋卵巢癌、胰腺癌、乳腺癌和前列腺癌。奧拉帕利銷售額逐年攀升,2020年銷售額高達25.01億美元。前列腺癌適應癥在中國的上市申請于6月21日獲批。
盧卡帕尼是美國批準的第二款PARP抑制劑,也是首個被批準用于治療前列腺癌的PARP抑制劑,獲批的適應癥包括卵巢癌和前列腺癌。目前市場表現一般,年銷售額還沒突破2億美元。
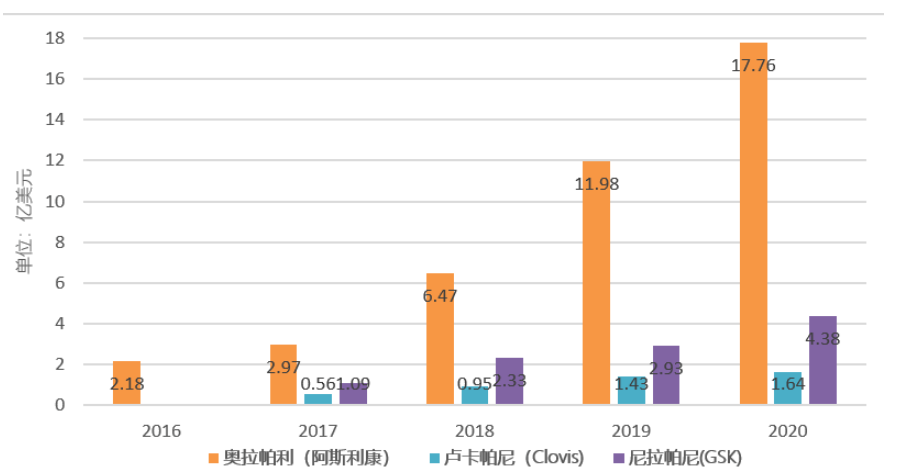
圖2 三大PARP抑制劑銷售額
表2 PARP抑制劑單藥用于mCRPC的II/III期試驗
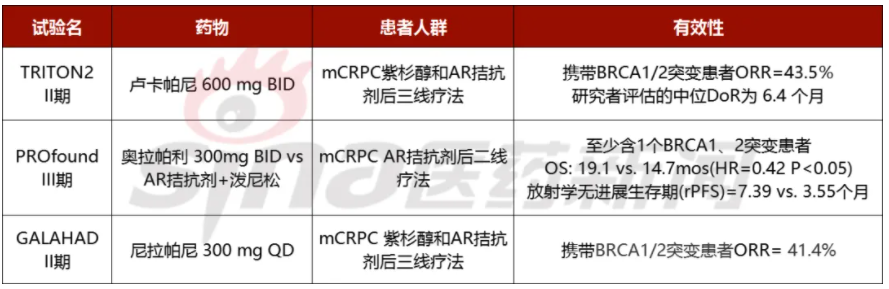
鑒于PARP抑制劑對后線療效已確證,PARP抑制劑相關聯用也在探索。包括PARP抑制劑+AR拮抗劑可能有協同作用,PARPi+AR抑制劑聯合方案一線/后線治療mCRPC能否進一步改善生存,尼拉帕利或奧拉帕尼+阿比特龍等試驗正在進行。另外,他拉唑帕尼和尼拉帕尼也都在進行與AR拮抗劑聯用于mHSPC人群的試驗。
在FDA批準PD-1抑制劑K藥(Pembrolizumab)用于存在MMR缺失的實體瘤后,NCCN指南建議通過檢測錯配修復及微衛星不穩定性篩選出的錯配修復缺陷(mismatch repair deficiency,dMMR)及微衛星高度不穩定(microsatellite instability-high,MSI-H)型前列腺癌患者再用K藥治療,這類人群在mCRPC中非常少,僅占2-5%,因此PARP抑制劑同樣也在嘗試與PD-1抑制劑聯用,也許可以拓寬適應癥。從機制上看,腫瘤突變負荷與DDR缺陷有關,特別是超突變腫瘤也常攜帶包括BRCA1/2的突變,PARP抑制介導的DNA損傷還會通過激活cGAS-STING通過增加T細胞浸潤入腫瘤細胞。奧拉帕利+durvalumab,奧拉帕利+Pembrolizumab, 盧卡帕尼+nivolumab,他拉唑帕尼+avelumab等均在進行mCRPC試驗。
PSMA靶向治療和其他激酶抑制劑
前列腺特異性膜抗原(PSMA)是一種跨膜糖蛋白,在超過80%的原發性和轉移性前列腺癌中都有表達,具有增殖促進的作用,其過表達還能夠使前列腺細胞擺脫對雄性激素的依賴。
諾華雖然在前列腺癌領域沒有產品,但希望能在放射性配體療法搶占先機。通過在2017和2018年收購Advanced Accelerator Applications 和Endocyte獲得靶向放射性療法產品,今年ASCO公布的Lutetium-177 PSMA 617 III期試驗結果,與單用最佳標準治療相比,mCRPC患者接受177Lu-PSMA-617聯合最佳標準治療的死亡風險降低38%(中位OS獲益4個月),其影像學進展或死亡風險降低60%(中位rPFS獲益5個月),2021年上半年將向美國和歐盟監管部門提交新藥注冊申請。
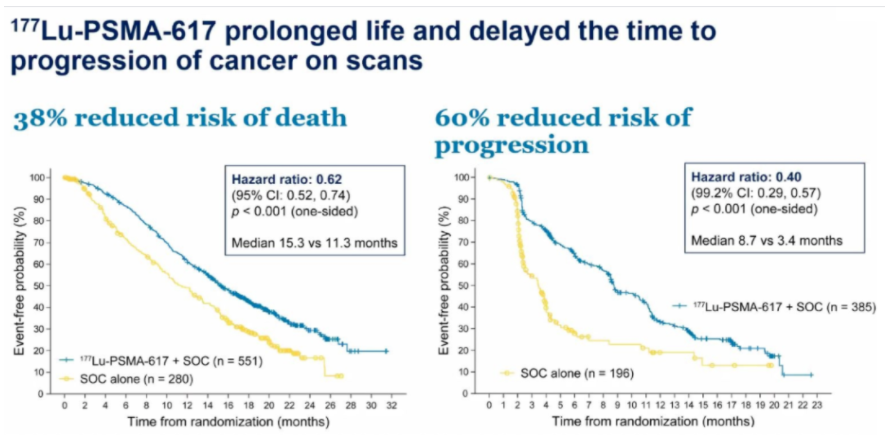
圖3 名為VISION的III期試驗試驗結果
拜耳除了進入目前mCRPC主要市場二代抗雄激素藥物市場外,也布局了PSMA靶向放射和與安進合作開發雙抗。2021年6月拜耳宣布將收購兩家專注開發放射配體療法的公司,分別為Noria Therapeutics和PSMA Therapeutics公司。通過收購拜耳將獲得基于同位素錒-225(actinium-225)的差異化α粒子療法的開發權益。
表3 主要臨床階段PSMA靶向治療
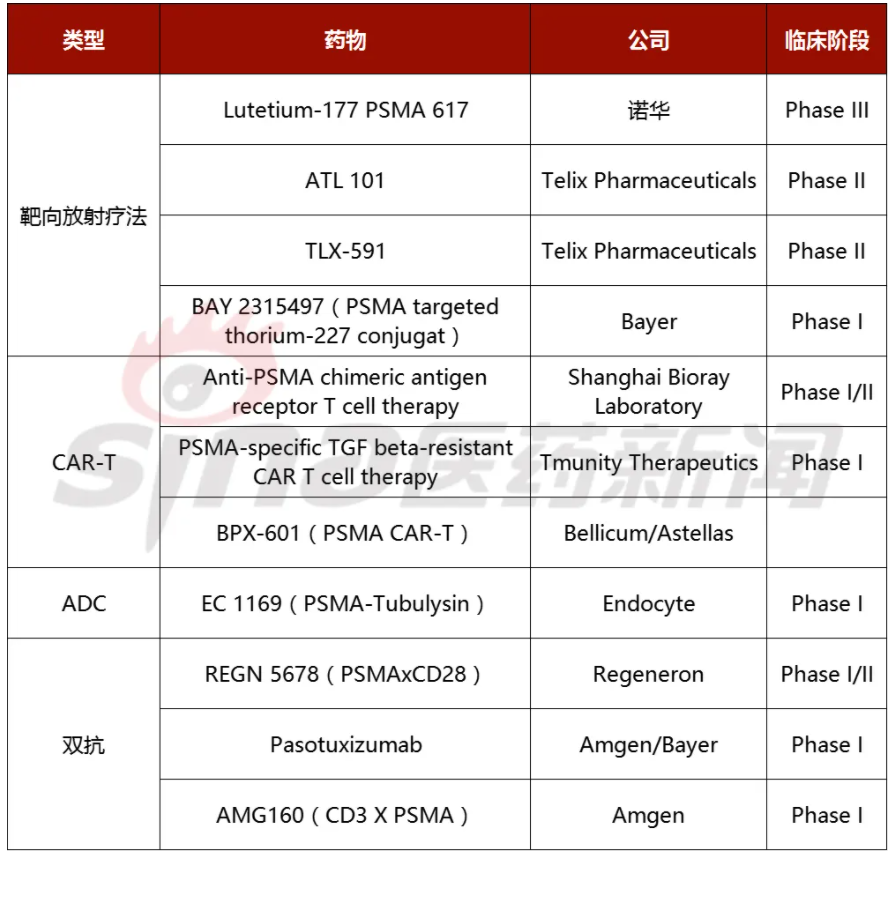
其他激酶抑制劑臨床開發得比較快的有Akt抑制劑和Cabozantinib,這兩類藥物也在面臨不同的挑戰。
Akt處于細胞生存通路PI3K/Akt/mTOR信號傳導通路的核心地位,與腫瘤細胞的發生、生長及轉移都緊密相關,并且在40-60%的mCRPC中發現PTEN缺失會導致PI3K/AKT通路激活,能不依賴于雄激素受體通路而促進前列腺癌細胞的生長,因此Akt抑制劑可能會對mCRPC患者有效。目前晚期臨床階段主要是羅氏的ipatasertib和AZ的capivasertib(AstraZeneca)。
羅氏并不是前列腺癌的玩家,Akt抑制劑研發多年一直沒有上市產品,但是去年ESMO公布了ipatasertib+阿比特龍+潑尼松對比阿比特龍+潑尼松用于mCRPC患者,納入了1101例患者,結果顯示雖然在所有人群中rPFS顯著改善,但在PTEN缺失患者中,ipatasertib組和安慰劑組的中位rPFS分別為18.5個月和16.5個月(HR=0.77,P=0.0335)。Capivasertib正在進行與阿比特龍聯用于PTEN缺失的mHSPC人群試驗(CAPItello-281)。目前看Akt抑制劑在mCRPC中的運用將受PTEN檢測的限制。
VEGFR、MET、AXL多靶點抑制劑Cabozantinib目前正在進行與羅氏的PD-L1抑制劑atezolizumab聯用對比AR拮抗劑用于AR拮抗劑經治的mCRPC患者的III期試驗(CONTACT-01)。目前公布過來自兩者聯用實體瘤試驗(Cosmic-021)中前列腺癌隊列患者的數據,在去年的ASCO會議上公布過36例患者的數據,ORR達33%,而今年公司公告的101例患者數據,獨立評審委員會評估ORR僅為18%,與PD-1單藥的結果相差不大,這一有效數據是否能支持加速審評仍待考證。
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容!