
2021-06-17 09:32:31來源:藥方舟瀏覽量:692
6月15日,中國國家藥監局藥品審評中心(CDE)最新公示,四川大冢制藥有限公司的阿立哌唑口服溶液,以符合兒童生理特征的兒童用藥品新品種、劑型和規格,被CDE納入優先審評,擬定適應癥為:6~17歲兒童和青少年的孤獨癥易激惹癥狀;6~17歲兒童和青少年的抽動穢語綜合征。
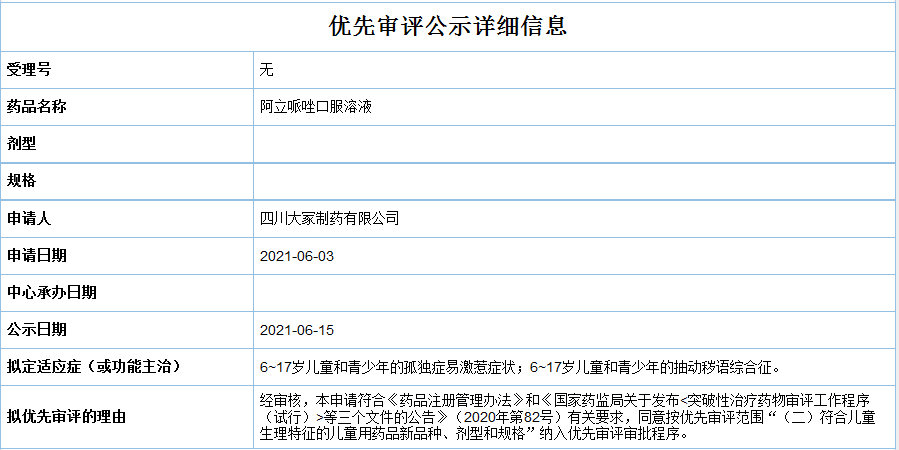
來源:CDE官網
阿立哌唑是全球首個上市的多巴胺(DA)-5羥色胺(5-HT)系統穩定劑,由大冢和靈北制藥聯合開發,用于精神分裂癥的治療。在美國,該產品還被批準用于治療自閉癥,它能夠改善患者易怒和刻板動作的癥狀。目前國內已有多款仿制藥獲批,涵蓋普通片劑、口崩片、膠囊劑、口服溶液等多種劑型,適應癥大多為精神分裂癥。
此次四川大冢制藥有限公司的阿立哌唑口服溶液擬納入優先審評,擬開發適應癥包括孤獨癥易激惹癥狀和抽動穢語綜合征。
孤獨癥又稱為自閉癥譜系障礙,是一種復雜的發育障礙,主要臨床癥狀包括缺乏社交能力、缺乏溝通能力、行為重復刻板、興趣范圍狹窄。據統計,大約有6.5%~8.1%的孤獨癥患兒伴有抽動穢語綜合征(又稱Tourette綜合征)。目前該治療領域的主要治療藥物為化學精神類藥物。
希望阿立哌唑口服溶液能早日在中國獲批,為患者帶來新的治療選擇。
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容!