目 錄
1. 國家醫保局:關于發布2024年國家醫保藥品目錄調整專家評審結果的公告
2. 國家藥監局藥審中心:關于發布2項指導原則的通告(2024年第38、39號)
3. 上海陽光醫藥采購網:關于規范注射劑掛網的工作提示
4. 貴州省醫保局:關于做好陜西九省聯盟部分藥品集中帶量采購協議期滿后接續采購中選結果執行工作的通知
5. 昆明市醫保局:昆明市第三批藥品帶量聯動采購藥品采購目錄變更的通告
1. 藥訊動態:重磅獲批
2. 藥訊動態:重磅臨床
3. 藥企動態:市場動態?
1. 胃潰瘍治療藥品銷售品種分析
2. 奧美拉唑零售放大市場銷售企業分析
3. 蘭索拉唑零售放大市場銷售企業分析
政策解讀

1、 國家醫保局:關于發布2024年國家醫保藥品目錄調整專家評審結果的公告
按照《2024年國家基本醫療保險、工傷保險和生育保險藥品目錄調整工作方案》,我局組織專家對2024年通過國家基本醫療保險、工傷保險和生育保險藥品目錄(簡稱2024年國家醫保藥品目錄)調整形式審查的申報藥品進行了評審。評審工作已結束,各相關申報企業可自行登陸國家醫保服務平臺(fuwu.nhsa.gov.cn)“2024年國家醫保藥品目錄調整申報”模塊查詢評審結果。具體信息請登錄國家醫保局官網查看。
2、國家藥監局藥審中心:關于發布2項指導原則的通告(2024年第38、39號)
 為鼓勵新藥研發,在國家藥品監督管理局的部署下,藥審中心組織制定了《地舒單抗注射液生物類似藥(腫瘤適應癥)臨床試驗指導原則(試行)》和《治療慢性心力衰竭藥物臨床試驗技術指導原則》(見附件)。根據《國家藥監局綜合司關于印發藥品技術指導原則發布程序的通知》(藥監綜藥管〔2020〕9號)要求,經國家藥品監督管理局審查同意,現予發布,自發布之日起施行。
為鼓勵新藥研發,在國家藥品監督管理局的部署下,藥審中心組織制定了《地舒單抗注射液生物類似藥(腫瘤適應癥)臨床試驗指導原則(試行)》和《治療慢性心力衰竭藥物臨床試驗技術指導原則》(見附件)。根據《國家藥監局綜合司關于印發藥品技術指導原則發布程序的通知》(藥監綜藥管〔2020〕9號)要求,經國家藥品監督管理局審查同意,現予發布,自發布之日起施行。
附件:1.地舒單抗注射液生物類似藥(腫瘤適應癥)臨床試驗指導原則(試行).pdf
2.治療慢性心力衰竭藥物臨床試驗技術指導原則.pdf

相關文件請掃描上方二維碼查看
3、上海陽光醫藥采購網:關于規范注射劑掛網的工作提示
根據《關于本市做好規范注射劑掛網工作的通知》(滬藥事藥品〔2024〕26號),要求已在上海市掛網的注射劑(含水針、粉針、輸液等各類注射劑)統一按照最小制劑單位(具體如支、瓶、袋等,組合包裝按套)重新申報掛網,不再按照實際包裝(如盒)掛網。內含包裝數量為“1”,包裝單位為“支/瓶/盒”的藥品編碼可暫不申請編碼轉換。具體信息請登錄上海陽光醫藥采購網官網查看。
4、貴州省醫保局:關于做好陜西九省聯盟部分藥品集中帶量采購協議期滿后接續采購中選結果執行工作的通知
為貫徹落實《國務院辦公廳關于推動藥品集中帶量采購工作常態化制度化開展的意見》(國辦發〔2021〕2號)等相關文件精神,根據《陜西省級(省際聯盟)部分藥品集中帶量采購協議期滿后接續采購文件》(SX-YPDL2023-01),現就做好陜西九省聯盟部分藥品集中帶量采購協議期滿后接續采購落地執行工作有關事項進行通知。具體信息請登錄貴州省醫保局官網查看。
附件:陜西九省聯盟藥品接續集采貴州省中選結果供應清單.xlsx

相關文件請掃描上方二維碼查看
5、昆明市醫保局:昆明市第三批藥品帶量聯動采購藥品采購目錄變更的通告
按照國家和省醫保局相關文件精神,昆明市醫療保障局于2024年9月14日發布了《昆明市第三批藥品帶量聯動采購工作方案》,由于藥品目錄中部分品種與外省近期集采目錄重復,現將昆明市第三批藥品帶量聯動采購藥品目錄變更如下,請企業根據最新藥品采購目錄(詳見附件)按照工作方案要求按時進行申報。具體信息請登錄昆明市醫保局官網查看。
行業動態

默沙東(MSD)抗PD-1單抗帕博利珠單抗(Keytruda)獲批新適應證,本次獲批的適應證為不可切除或轉移性黑色素瘤的一線治療。
禮來(Eli Lilly and Company)GIP/GLP-1受體雙重激動劑替爾泊肽注射液新適應癥上市申請獲得CDE受理,具體適應癥尚未披露。
齊魯制藥申報的司美格魯肽注射液的上市申請獲得CDE受理,具體適應癥尚未披露。
奧默醫藥和仙琚制藥共同申報的1類新藥奧美克松鈉注射液的上市申請獲得CDE受理。
樂普生物注射用維貝柯妥塔單抗擬納入優先審評,適用于既往經至少二線系統化療和PD-1/PD-L1抑制劑治療失敗的復發/轉移性鼻咽癌患者。
恒瑞醫藥提交的1類新藥瑞拉芙普-α注射液(SHR-1701)上市許可申請獲中國NMPA受理,本品聯合氟尿嘧啶類和鉑類藥物用于局部晚期不可切除、復發或轉移性胃及胃食管結合部腺癌的一線治療。
恒瑞醫藥1類新藥SHR-1905注射液獲批一項新的臨床試驗默示許可,擬開發用于12~17周歲的青少年哮喘患者。
上海醫藥申報的SPH4336片獲得一項新的臨床試驗默示許可,擬定適應癥為聯合奧希替尼治療KRAS突變型晚期實體瘤。
和記黃埔醫藥的化學1類新藥HMPL-760膠囊獲批一項新的臨床試驗默示許可,適應癥為聯合R-GemOx(利妥昔單抗+吉西他濱+奧沙利鉑)治療復發/難治彌漫大B細胞淋巴瘤(R/R DLBCL)。
普方生物申報的1類新藥注射用PRO1286獲得CDE批準臨床,擬用于治療實體瘤患者。
摯盟醫藥1類新藥CB03-154片獲批臨床,擬開發治療成人肌萎縮側索硬化(ALS)。
強生(Johnson & Johnson)申報的1類新藥bleximenib膠囊獲得CDE批準臨床,擬用于治療攜帶組蛋白-賴氨酸N-甲基轉移酶2A重排(KMT2Ar)或核磷蛋白1基因突變(NPM1m)的復發/難治性急性髓系白血病(AML)成人患者。
藥企動態:市場動態
9月17日,生物技術公司Capricor Therapeutics 宣布與日本新藥株式會社簽訂了具有約束力的條款清單。條款表示,日本新藥株式會社將在歐洲商業化和分銷 Capricor 的主要資產 deramiocel,用于治療杜氏肌營養不良癥 (DMD)。Capricor 將以 20% 的溢價獲得 1500 萬美元的股權投資,并在簽署最終協議后獲得 2000 萬美元的預付款,其中潛在里程碑金額高達 7.15 億美元,產品收入占比達到兩位數,綜合分銷協議的潛在里程碑目前總額約為 15 億美元。
9月18日,歐加農(Organon)宣布將收購Roivant子公司Dermavant Sciences。該交易預計將于2024年Q4完成。歐加農預計該交易不會導致其資本配置的優先級發生變化。根據協議條款,收購總交易額約為12億美元,包括1.75億美元的首付款、7500萬美元的監管里程碑付款以及9.5億美元的某些商業里程碑付款。此外,歐加農將向Dermavant Sciences股東支付凈銷售額的分層特許權使用費。交易完成后,作為收購價格對價的一部分,歐加農將承擔Dermavant Sciences的負債(截至2024年6月30日,負債約為2.86億美元)。
零售品類數據洞見

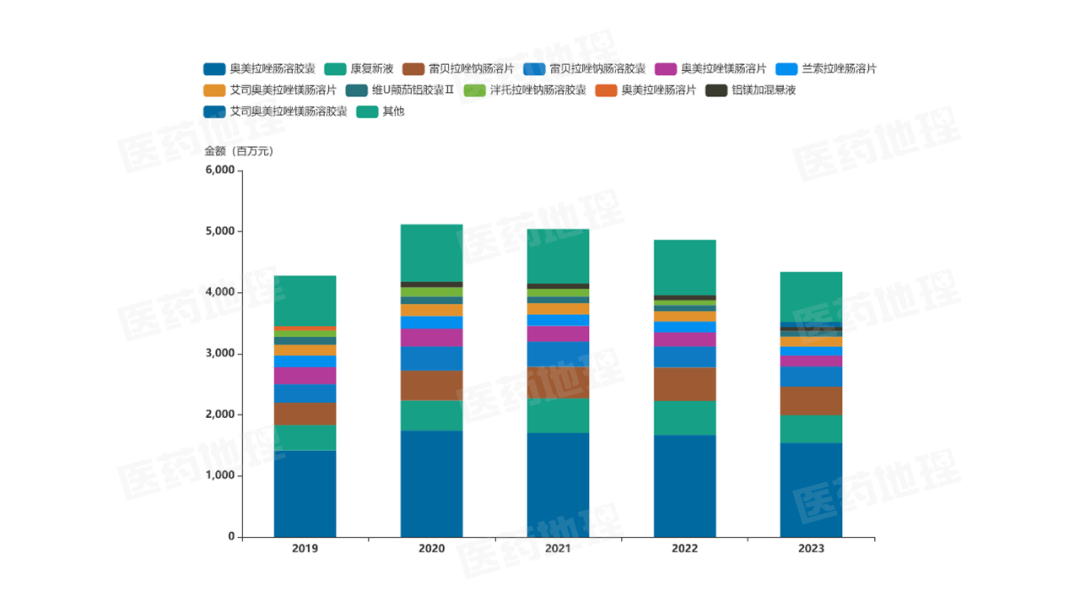
圖1:2019-2023年胃潰瘍治療藥品零售(放大市場)品種銷售額
數據來源: 中國藥品零售數據庫RPDB藥店數據
中國醫藥工業信息中心
胃潰瘍的病因與胃酸分泌合成過多、胃黏膜受損、幽門螺旋桿菌感染等因素有關,所以在治療方面,常用的治療方法有。所以在治療方面,可以分別針對病因進行抑酸治療、抗幽門螺桿菌(Hp)治療和治療胃黏膜保護治療。
奧美拉唑零售放大市場銷售企業分析
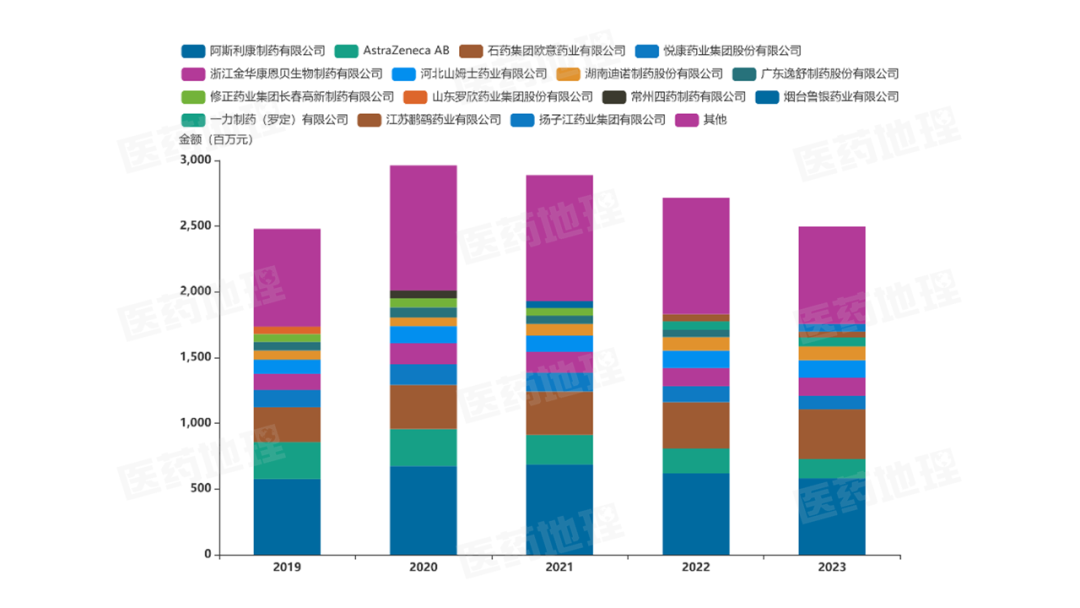
圖2: 2019-2023年奧美拉唑零售(放大市場)企業銷售額
數據來源: 中國藥品零售數據庫RPDB藥店數據
中國醫藥工業信息中心
奧美拉唑是一種抑酸藥,適用于治療胃潰瘍等上消化道疾病,也可用于胃酸相關癥狀的對癥治療,還可用于根除幽門螺桿菌、治療上消化道出血。根據PDB數據庫,奧美拉唑零售(放大市場)銷售額排名前三的企業分別是阿斯利康制藥有限公司、AstraZeneca AB和石藥集團歐意藥業有限公司。
蘭索拉唑零售放大市場銷售企業分析
 圖3: 2019-2023年蘭索拉唑零售(放大市場)企業銷售額
圖3: 2019-2023年蘭索拉唑零售(放大市場)企業銷售額
數據來源: 中國藥品零售數據庫RPDB藥店數據
中國醫藥工業信息中心
蘭索拉唑屬第二代新型質子泵抑制劑,可作為目前治療和酸分泌有關的各種消化道疾病的首選藥物。根據PDB數據庫,奧美拉唑零售(放大市場)銷售額排名前三的企業分別是湖南華納大藥廠股份有限公司、揚子江藥業集團四川海蓉藥業有限公司和辰欣藥業股份有限公司。
