
2024-07-08 17:39:50來源:藥方舟瀏覽量:1783
01 02 1、臨床用藥需要嚴格規定藥品用量,如果注射劑裝量過多又沒有科學合理的說明,則可能會引起給藥過量,產生嚴重毒副作用。 2、臨床用藥過程中,可能會產生將幾瓶藥物的剩余量被集中到一起湊成一個劑量的情況,很可能會引起嚴重微生物污染的風險。 注射劑一般包括大容量注射劑(50ml以上)、小容量注射劑(20ml以下)以及粉針劑三種劑型”。因此,大容量注射劑和小容量注射劑是以20ml為區分點,小容量注射劑的常規體積為1ml、2ml、5ml、10ml和20ml。
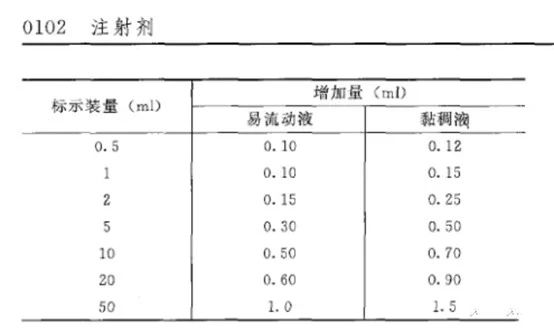
FDA于2022年推出的指南草案(MAPP)5019.1 Rev 1 《Allowable Excess Volume/Content in Injectable Drug and Biological Products》指出,應避免藥瓶中藥物裝量過多。該指南的目的旨在說明,在什么時機證明以及如何證明這種藥品灌裝過量是合理的。
《化學藥品注射劑仿制藥質量和療效一致性評價技術要求》(2020年第2號)(CDE發布20200514)指出仿制藥的過量灌裝量應與參比制劑保持一致。
USP43 General Chapter<1> Injections指出注射劑產品每個容器中的灌裝體積應略超過標簽的標示量。
ICH guideline Q8 (R2) on pharmaceutical development指出對于制劑生產過程中出現的過量現象,應提供如下信息:1)過量的量;2)過量的原因(如,補償生產過程中出現的損失);3)超出量的合理性說明,并應包含在制劑處方組成(3.2.P.3.2)中列出的原料藥的量中。
FDA2015年發布的 Guidance《Allowable Excess Volume and Labeled Vial Fill Size in Injectable Drug and Biological Products Guidance for Industry》指出In the case of drug products requiring reconstitution, the product should be designed to meet the label claim and acceptable overfill, and allow for correct dosing.對于需要復溶的藥物產品,產品的設計應符合標簽要求和可接受的過量灌裝,并允許正確的給藥。
主要內容,概述如下:
根據參比制劑說明書的用法進行復溶后,仿制藥最低灌裝量的復溶后藥物濃度應與說明書中規定的復溶后藥物濃度一致。
圖片來源:CDE官網
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容