
2020-12-18 17:00:33來源:DeepTech深科技 瀏覽量:701
死掉的細(xì)胞還能幫助治療急性骨髓性白血病(AML)?據(jù)了解,基于 AML 癌變細(xì)胞本身“骨髓歸巢”這一特點(diǎn),這種“死細(xì)胞”能夠運(yùn)載著藥物直達(dá)骨髓,也就是說,比傳統(tǒng)化療藥物使用更加精準(zhǔn),并可減低復(fù)發(fā)風(fēng)險(xiǎn)。

這是浙江大學(xué)藥學(xué)院顧臻教授的團(tuán)隊(duì)研究出的一種用于 AML 的全新療法,其巧妙的藥物遞送方法讓人聽聞后眼前一亮。相關(guān)論文也于 12 月 11 日登上《科學(xué)》子刊《Science Advances》的封面。

圖|《Science Advances》當(dāng)期封面
那死細(xì)胞是怎么傳遞藥物的呢?
簡單來說,首先需要從患者體內(nèi)提取出腫瘤細(xì)胞,再利用液氮在體外將腫瘤細(xì)胞“凍死”,隨后在含有死細(xì)胞的溶液中加入治癌藥物,比如阿霉素。如此,搭載藥物的“死細(xì)胞”就制備好了。
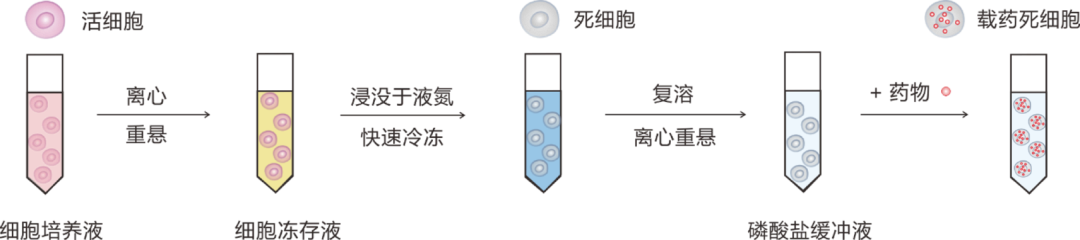
圖|死細(xì)胞制備流程圖
最后,再將這些載藥死細(xì)胞以靜脈注射的方式注射到患者體內(nèi)即可。這就是一次完整的治療過程。
方法雖好,不過離臨床試驗(yàn)還有一段距離,上述實(shí)驗(yàn)的研究對象也都是小鼠。DeepTech 向顧臻教授了解到,該團(tuán)隊(duì)很快就會在其它動(dòng)物模型上進(jìn)行實(shí)驗(yàn),以進(jìn)一步發(fā)掘其臨床應(yīng)用前景。
也許有人會好奇,被液氮凍死的細(xì)胞結(jié)構(gòu)不會被破壞嗎?這些細(xì)胞是否還會繼續(xù)增殖,又是否具有致病性呢?
載藥死細(xì)胞成功“歸巢骨髓”,顯著延長小鼠存活期
顧臻教授團(tuán)隊(duì)在《科學(xué)》子刊《Science Advances》上發(fā)表的這篇文章題為 Cryo-shocked cancer cells for targeted drug delivery and vaccination,論文第一作者為上海中醫(yī)藥大學(xué)中藥學(xué)院副教授慈天元博士及浙江大學(xué)藥學(xué)院特聘研究員李洪軍博士。

圖|刊登在《Science Advances》上的相關(guān)論文
基于 AML 癌變細(xì)胞本身“骨髓歸巢”這一特點(diǎn),該團(tuán)隊(duì)提出利用經(jīng)液氮處理的 AML 細(xì)胞的“死細(xì)胞”構(gòu)建具有骨髓靶向功能的遞藥系統(tǒng),以提高化療藥物在骨髓內(nèi)的富集、抑制 AML 細(xì)胞的增殖。
同時(shí)借助 AML“死細(xì)胞”本身所攜帶的腫瘤相關(guān)抗原,聯(lián)合免疫佐劑,刺激機(jī)體對 AML 癌細(xì)胞的特異性識別及殺傷。團(tuán)隊(duì)在小鼠模型上,驗(yàn)證了該平臺技術(shù)可聯(lián)合化療及免疫治療有效抑制腫瘤發(fā)展、提升生存率。
那么,回到前面的問題,被液氮凍死的細(xì)胞不會支離破碎嗎?答案是:不會。
在論文中,作者證實(shí)了死細(xì)胞具有與活細(xì)胞類似的細(xì)胞結(jié)構(gòu)。不過,實(shí)際上這一結(jié)論證實(shí)起來并不容易。
顧臻告訴 DeepTech,這的確是當(dāng)時(shí)團(tuán)隊(duì)攻克的一道難點(diǎn)。因?yàn)榧纫WC細(xì)胞徹底被“凍死”、不會復(fù)蘇,又要讓細(xì)胞盡可能保持完整的結(jié)構(gòu),在冷凍方式上著實(shí)難以把握。
經(jīng)過反復(fù)實(shí)驗(yàn),該團(tuán)隊(duì)終于得出結(jié)論,將 AML 細(xì)胞分散于特定的細(xì)胞凍存液并快速浸沒于液氮中 12 小時(shí),然后在 37℃ 的溫水中快速解凍,經(jīng)過液氮處理(liquid nitrogen-treated, LNT)的細(xì)胞就能“死得其所”。
如下圖所示,細(xì)胞雖死,卻有著相對完整的細(xì)胞骨架與細(xì)胞核。這不就可以成功“混入”活細(xì)胞的隊(duì)列中了。
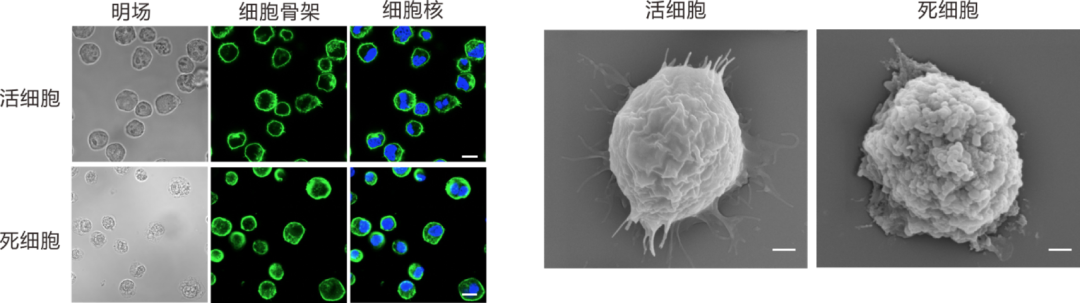
圖|死細(xì)胞的結(jié)構(gòu)表征:激光共聚焦顯微鏡(左),掃描電子顯微鏡(右)
由此表明,LNT 細(xì)胞具有與活細(xì)胞類似的細(xì)胞結(jié)構(gòu)。
但是接下來還需要評估 LNT 細(xì)胞的細(xì)胞活力,以驗(yàn)證其在體內(nèi)沒有致病性。對此,研究人員做了以下實(shí)驗(yàn),證實(shí)了與活細(xì)胞相比,LNT 細(xì)胞沒有表現(xiàn)出增殖活性,可作為化療藥物如阿霉素的遞藥載體。
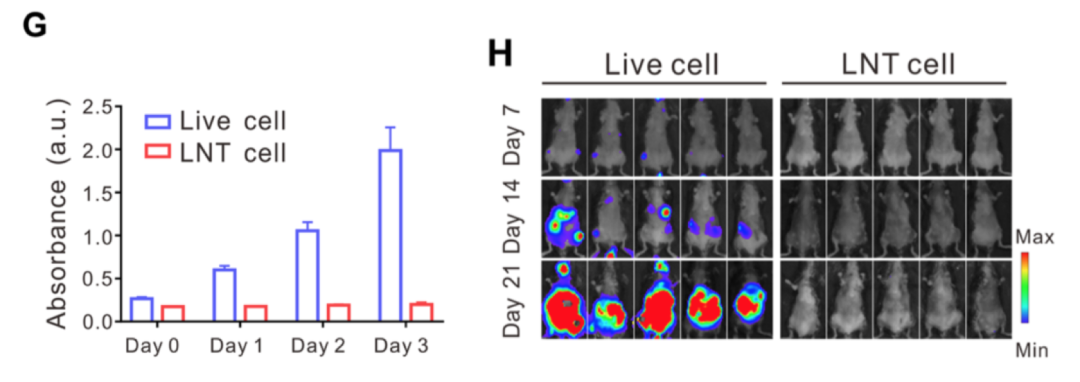
圖|圖 G 為用 CCK8 法對活細(xì)胞和 LNT 細(xì)胞進(jìn)行的細(xì)胞活力分析;圖 H 為用熒光素酶標(biāo)記的活細(xì)胞和 LNT 細(xì)胞在體內(nèi)的增殖情況
研究人員進(jìn)一步證實(shí)死細(xì)胞具有與源細(xì)胞類似的蛋白表達(dá),例如 AML 細(xì)胞株 C1498 的死細(xì)胞同樣攜帶 CD44 及 CXCR4 兩種與骨髓靶向密切相關(guān)的抗原,在一定程度上保留了 AML 活細(xì)胞的“骨髓歸巢”功能。
經(jīng) C1498 死細(xì)胞包載的阿霉素,與游離藥物相比具有更長的血液半衰期及更高的骨髓富集,與免疫佐劑聯(lián)用后,可顯著延長 AML 小鼠的生存期。
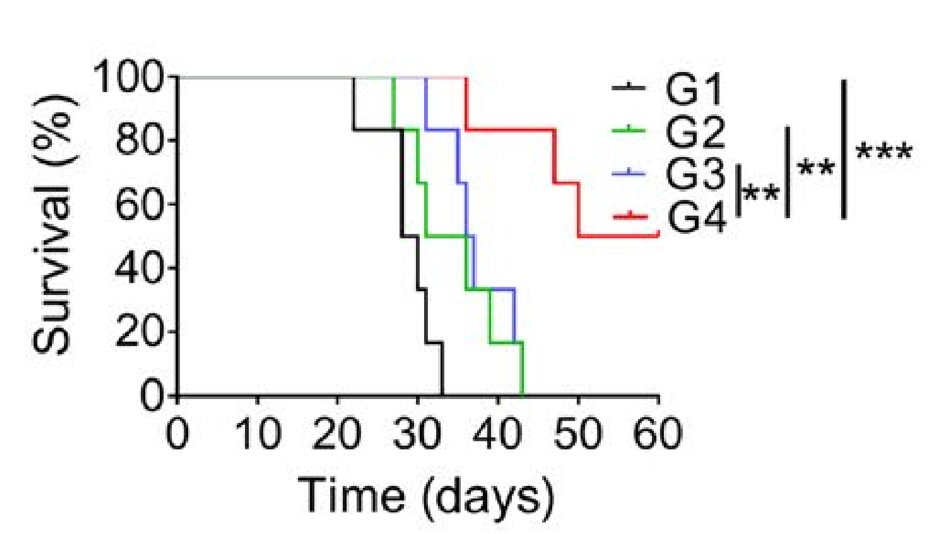
圖|載藥 LNT 腫瘤細(xì)胞聯(lián)合免疫佐劑顯著延長荷瘤小鼠存活率(G1: 生理鹽水; G2:阿霉素;G3:死細(xì)胞+免疫佐劑;G4:阿霉素/死細(xì)胞+免疫佐劑)
由此可見,該平臺技術(shù)可聯(lián)合化療及免疫治療有效抑制腫瘤發(fā)展、提升生存率。
那么,這項(xiàng)新療法到底強(qiáng)在哪里?
既有靶向性,又有“疫苗”效應(yīng)
了解這項(xiàng)新療法之前,首先需要了解一下什么是急性髓性白血病(AML)。AML 是一種髓系造血干細(xì)胞癌變的惡性疾病,表現(xiàn)為無法成熟的髓系癌細(xì)胞在骨髓內(nèi)大量增殖、聚集,導(dǎo)致骨髓正常的造血功能被抑制及其它生理機(jī)能的病變。
骨髓移植是治療 AML 的理想方法,但干細(xì)胞來源、數(shù)量、配型以及移植后的免疫排斥反應(yīng)等眾多問題往往限制了其廣泛應(yīng)用。化療是除骨髓移植外,AML 最為重要的治療手段之一,但化療愈后差、復(fù)發(fā)率高,五年生存期僅為 30%。
也就是說,常規(guī)化療很難清除骨髓里面的一些癌細(xì)胞,并且毒副作用明顯。而顧臻團(tuán)隊(duì)的這種靶向性更強(qiáng)的療法,理論上講相比傳統(tǒng)的化療可抑制復(fù)發(fā)。
顧臻教授對 DeepTech 說,“我們實(shí)際上就是通過這樣的方式直接用作 AML 的治療。一方面可以把化療的效果進(jìn)一步增強(qiáng);另一方面能夠進(jìn)一步刺激機(jī)體免疫,降低化療過后潛在的復(fù)發(fā)風(fēng)險(xiǎn)。”
簡而言之,從理論上講,采用這種“死細(xì)胞遞藥”的方式,可以為患者爭取更多的時(shí)間來采取進(jìn)一步的治療,而且毒副作用較小。
顧臻教授也向 DeepTech 透露,除了細(xì)胞具有靶向功能這一天然優(yōu)勢外,它還擁有較好的生物相容性(生命體組織對非活性材料產(chǎn)生反應(yīng)的一種性能),因?yàn)?/span>“細(xì)胞本身就來源于體內(nèi)”。
由此可見,相比合成材料制備的一些遞藥體系,以自身的細(xì)胞作為藥物載體具有一定優(yōu)勢。
另外,類比其他細(xì)胞療法,顧教授稱,該治療方案在質(zhì)量把控上潛在相對容易一些。“因?yàn)槌R?guī)的細(xì)胞療法需要取活的細(xì)胞,所以怎樣保證批次與批次之間的活性相仿,就需要一些非常細(xì)致標(biāo)準(zhǔn)的驗(yàn)證。”“現(xiàn)在這個(gè)細(xì)胞是死的,所以相對來說在質(zhì)量控制上面,難度或許會小一些。”
“自身細(xì)胞遞藥”這一平臺未來可期
據(jù)了解,接下來研究人員將對“死細(xì)胞療法”的抗癌有效性和安全性在動(dòng)物模型上做進(jìn)一步的系統(tǒng)評估,并與企業(yè)合作,推動(dòng)該創(chuàng)新技術(shù)臨床轉(zhuǎn)化的進(jìn)程。
在這項(xiàng)研究中,遞送的藥物是一種經(jīng)典的化療藥物阿霉素,當(dāng)然這只是作為一種藥物模型進(jìn)行的實(shí)驗(yàn)。顧教授表示,未來也可以換作其他的抗癌藥物,或者一些大分子藥物,包括抗體類的藥物等都可以進(jìn)行嘗試或組合嘗試,比如可以把一種藥物滲透到死細(xì)胞內(nèi)部,一種藥物放在細(xì)胞的表面,起到一個(gè)協(xié)同作用。
此外,DeepTech 也向顧臻教授了解到,團(tuán)隊(duì)正在拓展“利用液氮高效制備死細(xì)胞”的這一平臺技術(shù),有望用于其他疾病的治療,比如一些實(shí)體瘤的相關(guān)治療。

圖|顧臻教授(右)與團(tuán)隊(duì)成員
“我們強(qiáng)調(diào)的實(shí)際上是一個(gè)平臺技術(shù),通過很簡易的操作流程,可以把細(xì)胞凍死。但是細(xì)胞的形態(tài)還在,這樣一方面我們可以用作載藥,一方面細(xì)胞表面蛋白,比如抗原的活性還能夠保留下來,那么如果用作腫瘤治療的話,也能夠起到一個(gè)疫苗的作用。”顧教授告訴 DeepTech。
其實(shí)早在兩年前,顧臻教授的團(tuán)隊(duì)就研究出一種“聯(lián)合細(xì)胞藥物遞送”的 AML 治療方法,將藥物“搭載”在血小板上,再將血小板與造血干細(xì)胞相結(jié)合來遞藥。
相較于之前的研究,顧臻教授直言,“這次的設(shè)計(jì)相對簡單一些,直接用一種細(xì)胞就可以把藥物遞送過去。”在藥物模型的選擇方面,也與此前的研究不同,上次用到的是抗體藥物,而這次的阿霉素屬于小分子。
最后,顧臻教授表示出對“自身細(xì)胞遞藥”這種平臺技術(shù)的期待,并持以樂觀的態(tài)度。事實(shí)上,近年來顧教授的團(tuán)隊(duì)也在充分探尋我們體內(nèi)一些細(xì)胞具備的靶向功能,除了血小板、造血干細(xì)胞,甚至還研究過把抗癌藥載入脂肪細(xì)胞的油滴里來高效遞送藥物。
盡管從創(chuàng)新研發(fā)到投產(chǎn)還有很長一段路要走,顧教授也表示一直在努力推進(jìn),想辦法轉(zhuǎn)化。如他所言:“我認(rèn)為在藥物遞送平臺設(shè)計(jì)上面,可以做的事情特別多。而且從轉(zhuǎn)化這個(gè)角度來講,因?yàn)檫@些凍死的細(xì)胞都源于體內(nèi),副作用小,并且在量產(chǎn)、質(zhì)控方面有潛在的優(yōu)勢。
聲明:本文系藥方舟轉(zhuǎn)載內(nèi)容,版權(quán)歸原作者所有,轉(zhuǎn)載目的在于傳遞更多信息,并不代表本平臺觀點(diǎn)。如涉及作品內(nèi)容、版權(quán)和其它問題,請與本網(wǎng)站留言聯(lián)系,我們將在第一時(shí)間刪除內(nèi)容!