
2024-06-04 09:59:01來源:美柏必締 瀏覽量:918
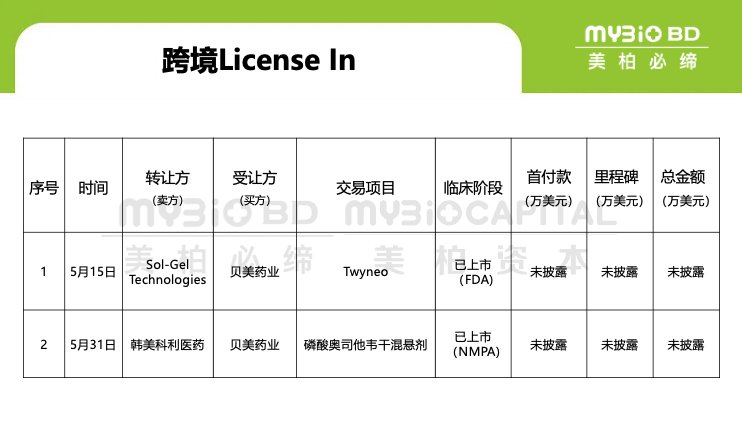
據(jù)不完全的統(tǒng)計,2024年5月中國醫(yī)藥BD及并購交易共計15筆,其中跨境資產(chǎn)買入2筆,跨境資產(chǎn)賣出9筆,中國境內(nèi)交易4筆。
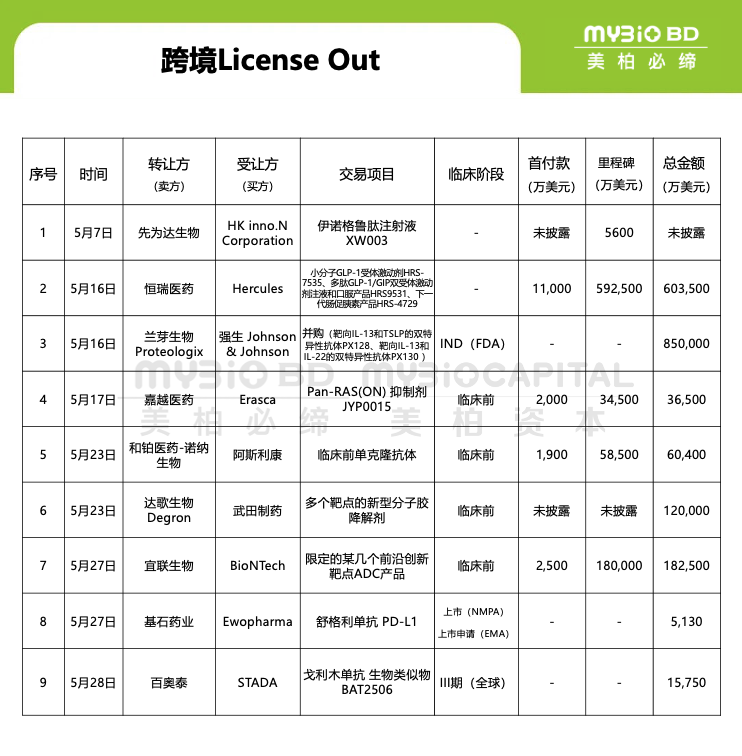
2024年5月16日,恒瑞醫(yī)藥發(fā)布公告,將GLP-1產(chǎn)品組合的大中華區(qū)外全球權(quán)益授權(quán)給美國Hercules公司。交易的GLP-1產(chǎn)品組合包括小分子GLP-1受體激動劑HRS-7535,GLP-1R/GIPR雙靶點(diǎn)激動劑、下一代腸促胰素產(chǎn)品HRS-4729。Hercules是一家今年5月剛剛成立的公司,由貝恩資本、Atlas Ventures、RTW資本、Lyra資本聯(lián)合出資4億美元,作為交易對價一部分,恒瑞獲得Hercules19.9%的股權(quán)。恒瑞醫(yī)藥還將獲得首付款和近期里程碑總計1.1億美元,2億美元臨床及監(jiān)管里程碑金額,累計不超過57.25億美元銷售里程碑金額,低個位數(shù)至低兩位數(shù)比例的銷售額提成,協(xié)議總金額60.35億美元。
2024年5月16日,蘇州蘭芽生物制藥Proteologix宣布其已達(dá)成最終協(xié)議, 將被強(qiáng)生公司(Johnson & Johnson)以8.5億美元現(xiàn)金收購, 并有可能獲得額外的一定金額的里程碑付款。Proteologix的產(chǎn)品組合包括正準(zhǔn)備進(jìn)入一期臨床開發(fā)的PX128和處于臨床前開發(fā)階段的PX130。PX128是一款靶向IL-13和TSLP的雙特異性抗體, 用于治療中重度特應(yīng)性皮炎 (AD) 和中重度哮喘; PX130是一款靶向IL-13和IL-22的雙特異性抗體, 用于治療中重度AD。由于AD和哮喘都是異質(zhì)性疾病, 不同的患者亞群存在不同的致病通路, 因此靶向多條通路有望實(shí)現(xiàn)高水平的療效和緩解。除PX128和PX130外, 此次收購還將為強(qiáng)生公司提供可用于多種其他疾病的其他雙特異性抗體項(xiàng)目。
2024年5月17日,嘉越醫(yī)藥與美國Erasca, Inc. (Nasdaq:ERAS) 共同宣布簽署一項(xiàng)Pan-RAS(ON) 抑制劑JYP0015項(xiàng)目授予Erasca中國內(nèi)地和中國港澳之外的全球獨(dú)家授權(quán)協(xié)議。這一具有里程碑意義的授權(quán)協(xié)議將促進(jìn)兩家企業(yè)更好地為全球尚未滿足臨床需求的胰腺癌(PDAC)、結(jié)直腸癌(CRC)、非小細(xì)胞肺癌(NSCLC)等適應(yīng)癥的患者帶來高效、安全的醫(yī)療解決方案。根據(jù)協(xié)議條款,ERASCA將獲得JYP0015中國內(nèi)地和中國港澳之外的全球獨(dú)家研究、開發(fā)和商業(yè)化的授權(quán)許可。嘉越醫(yī)藥將有資格獲得首付及潛在近期付款高達(dá)2000萬美元,總計最高達(dá)3.45億美元的潛在開發(fā)、商業(yè)化里程碑及全球行使權(quán)付款等,以及凈銷售額的分級特許權(quán)使用費(fèi)。
2024年5月23日,和鉑醫(yī)藥(股票代碼:02142.HK)全資子公司蘇州諾納生物宣布,與阿斯利康就臨床前單克隆抗體項(xiàng)目達(dá)成許可協(xié)議,加速腫瘤靶向療法的開發(fā)。根據(jù)協(xié)議,諾納生物在交易完成后將獲得1900萬美元首付款,并有權(quán)獲得1000萬美元可預(yù)期的近期里程碑付款,以及高達(dá)5.75億美元開發(fā)、監(jiān)管及商業(yè)里程碑付款和基于凈銷售額的分級特許權(quán)使用費(fèi)。此外,如果阿斯利康行使選擇權(quán),諾納生物將進(jìn)一步獲得相關(guān)付款。
2024年5月23日,達(dá)歌生物(Degron Therapeutics)宣布與武田制藥簽訂了合作開發(fā)及獨(dú)家許可協(xié)議,以發(fā)現(xiàn)和開發(fā)用于腫瘤學(xué)、神經(jīng)科學(xué)和炎癥領(lǐng)域多個靶點(diǎn)的新型分子膠降解劑。根據(jù)協(xié)議條款,達(dá)歌生物將獲得首付款,并有資格獲得未來潛在的臨床前、臨床開發(fā)和商業(yè)化里程碑的付款,總額最高可達(dá)12億美元。除此之外,達(dá)歌生物還有資格獲得任何潛在商業(yè)化產(chǎn)品的銷售特許權(quán)使用費(fèi)。雙方可以選擇擴(kuò)大合作范圍,以納入更多靶點(diǎn)。此外,武田將對達(dá)歌生物進(jìn)行股權(quán)投資。達(dá)歌生物仍然保留其自有管線的全部所有權(quán)。達(dá)歌生物將利用其GlueXplorer?平臺,針對武田選定的特定疾病靶點(diǎn)發(fā)現(xiàn)、驗(yàn)證和優(yōu)化分子膠降解劑。在達(dá)到一定進(jìn)展階段后,這些項(xiàng)目將移交給武田進(jìn)行進(jìn)一步開發(fā)和商業(yè)化。
2024年5月27日,蘇州宜聯(lián)生物宣布與BioNTech達(dá)成一項(xiàng)新的戰(zhàn)略合作。BioNTech將獲得一項(xiàng)利用宜聯(lián)生物TMALIN? ADC技術(shù)平臺開發(fā)針對限定的某幾個前沿創(chuàng)新靶點(diǎn)的ADC產(chǎn)品的獨(dú)家選擇權(quán)及相應(yīng)全球獨(dú)家許可。根據(jù)新協(xié)議條款,宜聯(lián)生物將獲得2500萬美元的首付款,并有資格獲得最高可達(dá)18億美元的開發(fā)、監(jiān)管和商業(yè)化里程碑付款,以及未來基于全球年度銷售凈額的梯度特許權(quán)使用費(fèi)。作為協(xié)議的一部分,宜聯(lián)生物將享有BioNTech未來尋求這些ADC產(chǎn)品在大中華區(qū)(中國大陸、香港、澳門、臺灣)任一或多個地區(qū)市場對外授權(quán)或轉(zhuǎn)讓時的優(yōu)先合作權(quán)。2023年10月,宜聯(lián)生物與BioNTech就YL202/BNT326,一款靶向HER3的ADC項(xiàng)目達(dá)成戰(zhàn)略合作和全球許可協(xié)議,雙方?jīng)Q定進(jìn)一步拓展合作范圍,并達(dá)成了本次平臺合作許可協(xié)議。
2024年5月27日,基石藥業(yè)宣布已與歐洲制藥公司 Ewopharma 建立戰(zhàn)略商業(yè)化合作伙伴關(guān)系,將舒格利單抗在中歐和東歐的商業(yè)化權(quán)利授予 Ewopharma。根據(jù)這項(xiàng)許可和商業(yè)化協(xié)議,Ewopharma 將獲得舒格利單抗在瑞士以及 18 個中東歐國家 (CEE) 的商業(yè)化權(quán)。這包括歐盟成員國保加利亞、克羅地亞、捷克共和國、愛沙尼亞、匈牙利、拉脫維亞、立陶宛、波蘭、羅馬尼亞、斯洛伐克和斯洛文尼亞,以及非歐盟國家阿爾巴尼亞、波斯尼亞和黑塞哥維那、科索沃、北馬其頓、摩爾多瓦、黑山和塞爾維亞。基石藥業(yè)制藥公司將獲得高達(dá) 5130 萬美元(相當(dāng)于約 3.7 億美元)的首期付款以及后續(xù)的注冊和銷售里程碑付款。基石藥業(yè)將通過向 Ewopharma 銷售產(chǎn)品獲得國際收入,Ewopharma 將負(fù)責(zé)定價、報銷、營銷、分銷和其他相關(guān)事宜,基石藥業(yè)將負(fù)責(zé)供應(yīng)產(chǎn)品并為相關(guān)品牌提供必要的培訓(xùn)和支持。
2024年 5月28日,百奧泰宣布已與STADA公司就BAT2506(一款參照欣普尼開發(fā)的戈利木單抗生物類似藥)簽署授權(quán)許可及商業(yè)化協(xié)議。根據(jù)協(xié)議條款,百奧泰將負(fù)責(zé)BAT2506的研發(fā)、生產(chǎn)以及商業(yè)化供應(yīng),STADA將負(fù)責(zé)BAT2506在歐盟、英國、瑞士以及其他部分歐洲國家市場的商業(yè)化。在達(dá)到相應(yīng)的里程碑事件后,百奧泰可獲得首付款加上里程碑款總金額最高至1.575億美元,以及凈銷售額的兩位數(shù)百分比作為收入分成。

2024年5月7日,通化東寶與北京質(zhì)肽生物關(guān)于GLP-1產(chǎn)品司美格魯肽注射液簽署了《商業(yè)化授權(quán)及MAH合作協(xié)議》(以下簡稱“協(xié)議”)。根據(jù)協(xié)議約定,公司將獲得質(zhì)肽生物臨床在研產(chǎn)品ZT001司美格魯肽注射液(適應(yīng)癥:成人2型糖尿病患者控制血糖)(以下簡稱“合作產(chǎn)品”)中國大陸地區(qū)獨(dú)占商業(yè)化權(quán)益,以及共同合作開發(fā)海外市場權(quán)利。合作產(chǎn)品在中國大陸地區(qū)已完成2型糖尿病適應(yīng)癥的I期臨床,并已啟動III期臨床研究。
2024年5月7日,通化東寶藥業(yè) 與君合盟生物制藥及其原股東簽署《君合盟生物制藥(杭州)有限公司之增資協(xié)議》。根據(jù)協(xié)議,公司擬以自有資金人民幣1億元認(rèn)購君合盟,新增注冊資本950.31萬元,剩余部分計入資本公積,占君合盟增資擴(kuò)股后總股本的8.6759%。本次投資入股君合盟, 符合公司創(chuàng)新研發(fā)、對外合作的戰(zhàn)略發(fā)展方向。君合盟主要從事重組蛋白質(zhì)創(chuàng)新藥物的開發(fā)及合成生物學(xué)領(lǐng)域創(chuàng)新產(chǎn)品開發(fā),擁有國內(nèi)領(lǐng)先的的技術(shù)開發(fā)平臺及完整的產(chǎn)品開發(fā)體系,現(xiàn)有重組人生長激素、重組長效生長激素、重組A型肉毒毒素、重組I型人膠原蛋白、重組III型人膠原蛋白共5條研發(fā)管線。通過此次增資,公司將獲得君合盟現(xiàn)有的及未來的研發(fā)項(xiàng)目在全球范圍內(nèi)的各類開發(fā)及商業(yè)合作優(yōu)先權(quán),將有助于未來公司業(yè)務(wù)范圍延伸至消費(fèi)醫(yī)療領(lǐng)域,產(chǎn)品體系進(jìn)一步豐富與多元化,有利于改善公司收入結(jié)構(gòu),提升持續(xù)盈利能力。本次增資后,公司亦將利用自身資本、研發(fā)、臨床等方面的優(yōu)勢與資源,積極推進(jìn)君合盟管線的研發(fā)進(jìn)程,協(xié)助其盡快實(shí)現(xiàn)相關(guān)技術(shù)的產(chǎn)業(yè)化。
2024年5月23日,佑嘉(杭州)生物醫(yī)藥科技有限公司(以下簡稱:佑嘉生物)與四川瀘州步長生物制藥有限公司 (以下簡稱:步長生物)于北京正式簽署《靶向治療心血管靶點(diǎn)的小干擾RNA(siRNA)創(chuàng)新藥項(xiàng)目開發(fā)合同》,并由佑嘉生物授予步長生物獨(dú)家許可合作權(quán)益,共同推進(jìn)創(chuàng)新藥物臨床轉(zhuǎn)化、拓展心血管疾病防治新篇章。
2024年05月28日,三生制藥(01530.HK)宣布,旗下子公司浙江三生蔓迪藥業(yè)與深圳翰宇藥業(yè)就司美格魯肽注射液產(chǎn)品達(dá)成合作。雙方將圍繞該產(chǎn)品藥物開發(fā)、臨床研究、注冊申報、大健康渠道、以及品牌打造等環(huán)節(jié)進(jìn)行協(xié)同,共同開拓其商業(yè)版圖。根據(jù)協(xié)議,三生蔓迪與翰宇藥業(yè)將聚焦用于減肥的司美格魯肽注射液在減重適應(yīng)癥,構(gòu)建廣泛的業(yè)務(wù)合作關(guān)系。本次合作模式包括交易對價、獨(dú)家供應(yīng)、以及后端分成。三生蔓迪將向翰宇藥業(yè)支付最高人民幣2.7億元里程碑付款,其中包含人民幣4,500萬元的臨床前技術(shù)成果對價款,此外三生蔓迪還將向翰宇藥業(yè)支付獨(dú)家采購價以及約兩位數(shù)以毛利為基礎(chǔ)計算的銷售提成。三生蔓迪在大健康領(lǐng)域線上線下的渠道實(shí)力與翰宇藥業(yè)多肽藥物研發(fā)經(jīng)驗(yàn)形成強(qiáng)強(qiáng)聯(lián)合之勢,為國內(nèi)廣大具有體重管理需求的人群提供有效解決方案。
2024年截止5月底,中國醫(yī)藥領(lǐng)域共完成75筆交易(跨境引進(jìn)18筆,跨境出海39筆,中國境內(nèi)交易18筆)。同比2023年前5個月的53筆交易(跨境引進(jìn)14筆,跨境出海 24筆,境內(nèi)交易15筆),同比增長41.5%,交易數(shù)量增長明顯。國內(nèi)制藥行業(yè)在一二級市場及醫(yī)藥政策持續(xù)收緊背景下,加速外部合作。
聲明:本文系藥方舟轉(zhuǎn)載內(nèi)容,版權(quán)歸原作者所有,轉(zhuǎn)載目的在于傳遞更多信息,并不代表本平臺觀點(diǎn)。如涉及作品內(nèi)容、版權(quán)和其它問題,請與本網(wǎng)站留言聯(lián)系,我們將在第一時間刪除內(nèi)容