上期文章,鼎泰團隊對臨床試驗失敗的6款siRNA藥物及失敗原因進行了復盤分析(點擊查看原文),同時也借鑒這些案例啟發我們如何在siRNA藥物早期研究中更好地進行非臨床藥效學研究和概念驗證試驗。
siRNA藥物通過調控mRNA增加或減少疾病相關蛋白的產生而發揮藥理學活性。評價mRNA 和蛋白水平的變化,需建立合適的體外和體內模型?除了已被業界所熟知的基于LNP遞送系統和GalNac偶聯技術以外,對于肝外靶向遞送、新型作用機制的siRNA藥物,藥效學研究或藥代動力學/藥效學(PK/PD)具有更為重要的意義。
與小分子藥物和蛋白類藥物不同, siRNA藥物 PK/PD 關系獨特:
血漿中暴露時間短、靶器官(如肝臟)中暴露時間長且藥效作用持久
圖1. Givosiran、Inclisiran 和 Vutrisiran:血漿中siRNA濃度和血清中PD標志物變化關系[1]
關鍵的藥效學物質基礎是胞漿中siRNA和RISC復合物,而非血漿或靶器官中總的siRNA濃度
圖2. 肝臟中siRNA總濃度、siRNA-RISC濃度和PD標志物變化關系[1]
siRNA的內體逃逸效率、siRNA與RISC的結合動力學也可能因平臺或遞送系統而異
圖3. GalNac siRNA進入細胞、細胞內分布和發揮藥理學活性的過程和關鍵步驟[2]
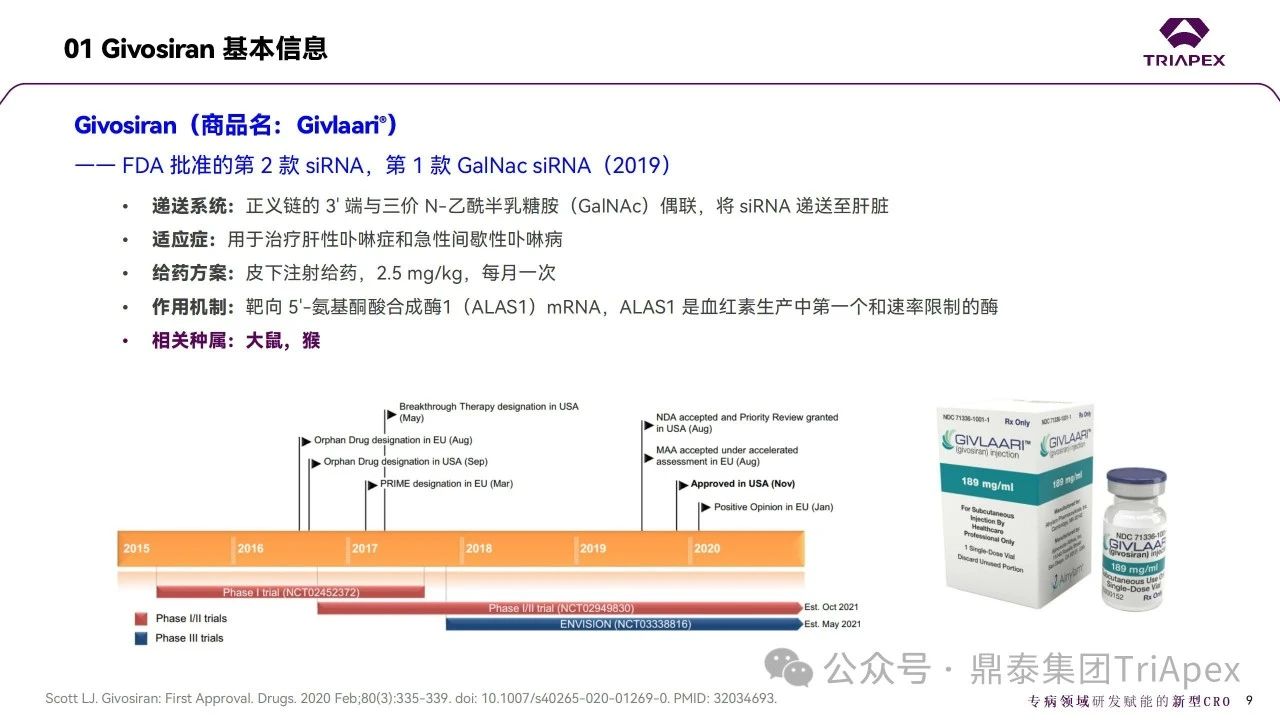
圖4. 兩種方案可提高 siRNA 內體逃逸效率[3]
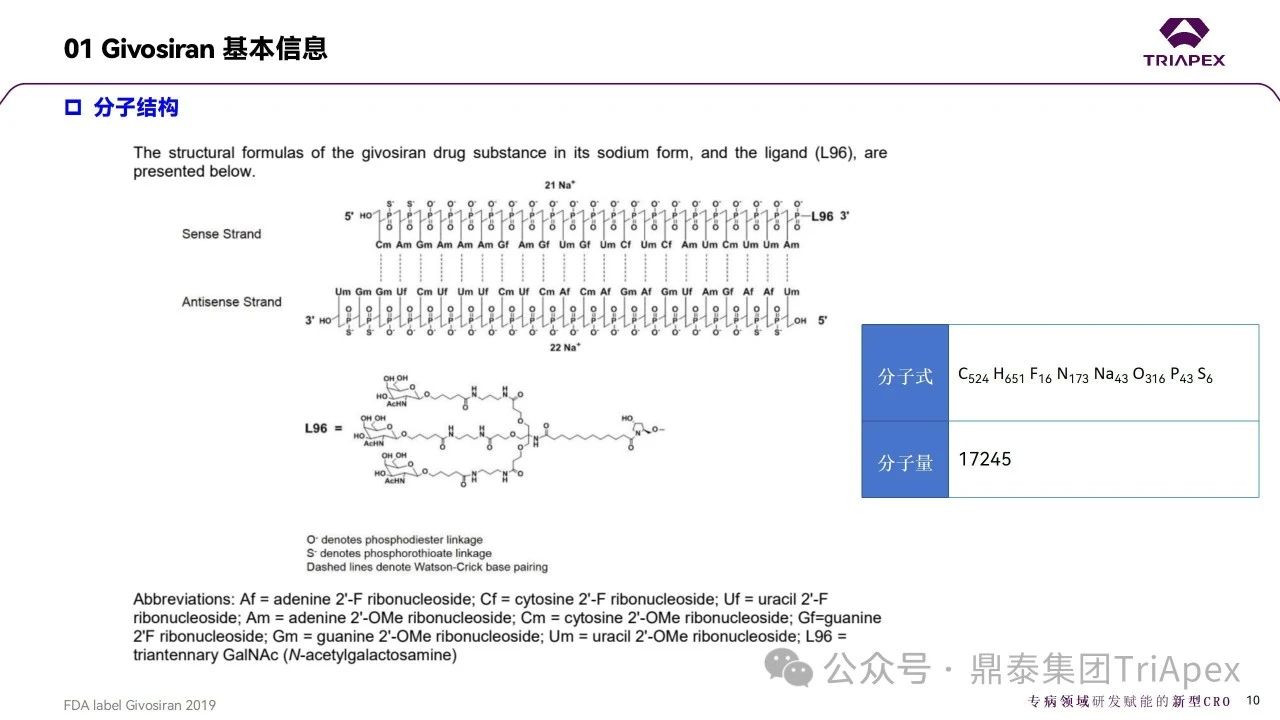
上述特點使得siRNA藥物的藥效學評價和臨床轉化面臨較大的挑戰。未來需要開展更多關于siRNA藥物作用機制和PK過程(包括細胞內PK)的定量研究,以獲得更加精準的用于提示臨床有效性和指導臨床試驗設計的非臨床藥效學數據。此外,整合已有的非臨床和臨床數據對模型進行改進和優化同樣重要。
本文對已獲得FDA批準上市的6款siRNA藥物(截至2024年2月)的非臨床藥效學研究進行了匯總(文末查看),并簡要總結了設計要點和研究思路。
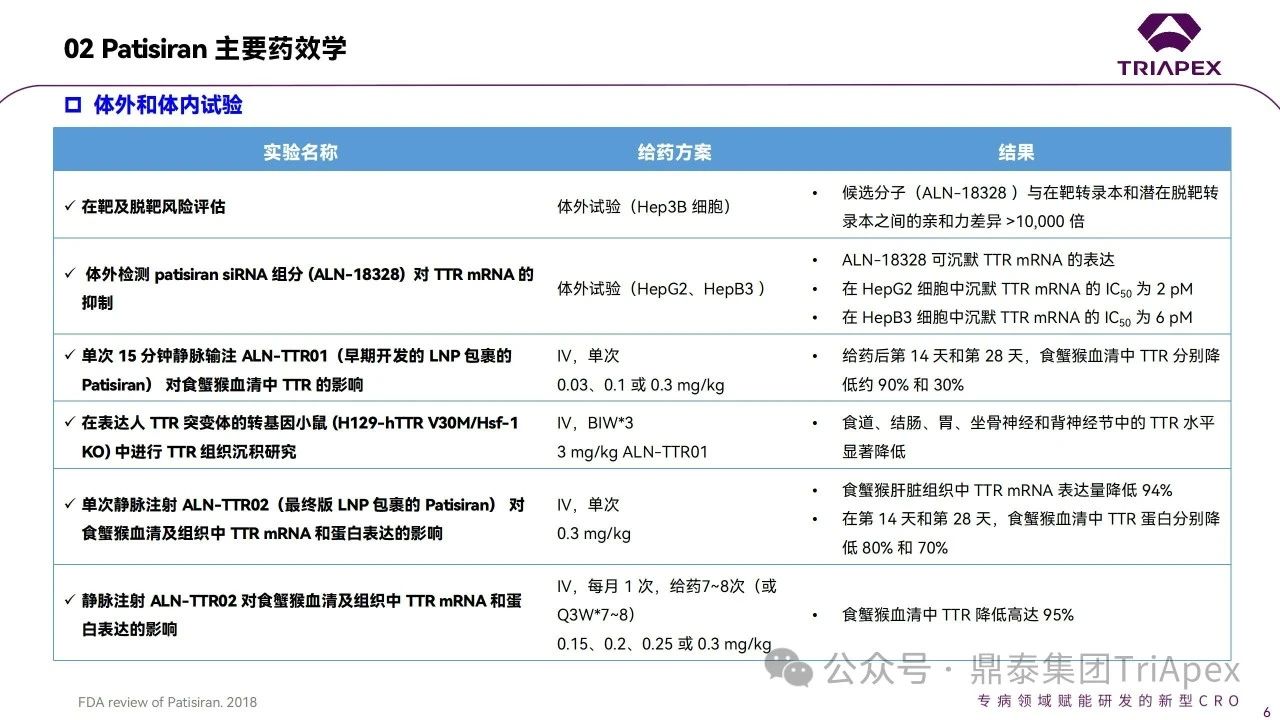
體外試驗是siRNA藥物研發的重要環節,用于篩選靶向特異性強、活性高的siRNA序列。通常,選擇人或動物的原代細胞?細胞系或轉染的細胞系作為試驗體系,考察siRNA對細胞活性?功能?相關蛋白和靶mRNA 水平的影響?借助體外試驗,除了可考察對人體靶點的作用外,還能評估對不同種屬mRNA的影響,為毒理學試驗中相關種屬的選擇提供依據?根據FDA審評報告,已上市的6款siRNA藥物均可濃度依賴性地調控靶mRNA并改變蛋白表達水平,產生體外活性;均在猴體內表現出藥理學活性?
表1. 已上市siRNA藥物相關種屬匯總
此外,借助在線工具(in silico)對不同種屬間靶mRNA的同源性進行比對或預測其與候選siRNA藥物的配對情況,為相關種屬的選擇提供參考;對人轉錄本中可能與候選siRNA藥物發生雜交的非目標序列(脫靶序列)進行初步篩選,然后進行進一步的體外試驗和/或更全面的風險評估(siRNA候選分子多層級脫靶效應評估策略,發表中)。
siRNA藥物與靶mRNA 的配對具有很高的特異性,只有與靶mRNA同源性高的序列才能配對成功。通常,通過1中所述手段進行相關種屬的選擇,然后在相關種屬動物中開展體內藥效學研究;非人靈長類動物是評價siRNA藥物體內藥效學的重要模型,可以確定有效劑量范圍并評估給藥方案。如沒有可產生藥理學活性的相關種屬,可選擇轉基因動物模型,或開展相應的體外藥效學試驗?
通過體內藥效學試驗,可對劑量-效應關系、時間-效應關系、療效相關生物標志物等進行探索。此外,從定量藥理的角度,PK/PD模型、劑量-效應-時間模型、PK/PB模型等在siRNA藥物開發中發揮著重要作用,可用于將藥物研發從臨床前到臨床各階段的數據進行模擬、外推和預測。對于研發者充分理解和利用siRNA藥物獨特的PK/PD關系、指導siRNA藥物的開發至關重要。科學合理地設計臨床前藥效學試驗,結合轉化角度的研究,可以更好地支持siRNA產品的臨床試驗設計和人體療效預測,有助于確定臨床首次人體試驗(FIH)及不同臨床階段的給藥方案,并用于NDA申請時作為支持臨床劑量選擇依據的描述。已上市siRNA藥物,如patisiran和givosiran的上市批準均采用了上述藥效學模型。
圖5. Givosiran劑量-尿ALA/PBG水平(上)、劑量-尿ALAS1 mRNA/ALA/RBG水平(中)、劑量-尿ALA/PBG水平(下)相關性分析[4]
在嚴格遵守動物實驗倫理規范和不同國家藥品監管要求的前提下,鼎泰集團依托豐富的非人靈長類動物疾病模型資源、專業的小核酸藥物藥效學、DMPK 和安全性評價經驗,將持續高效助力國內外siRNA 藥物的轉化研究、臨床開發和注冊申報。
鼎泰集團子公司昆明科靈(KBI)在非人靈長類動物疾病模型藥效學研究方面積累了豐富經驗。依靠資源和技術優勢,我們已經建立了多種自發性或誘導性非人靈長類動物疾病模型(恒河猴、食蟹猴,詳見圖6),這些模型具有與人同源性高、疾病的基因型和表型與疾病人群更為接近的優點。
圖6. 鼎泰集團已經建立多種適用于siRNA藥物藥效學研究的非人靈長類疾病動物模型
在siRNA領域,KBI常年與多家國內外領先核酸藥物公司保持緊密合作。截至目前, KBI已完成了 30 多項siRNA藥物的概念驗證試驗和臨床前藥效學研究,其中涵蓋諸如高血脂、NASH、高血壓等多個熱門適應癥。同時, KBI緊密跟進行業研發趨勢和臨床需求,借助鼎泰集團戰略性優勢,持續加強在新技術領域的前瞻性布局和技術能力建設,致力于滿足不同客戶在創新siRNA藥物(包括新的適應癥、遞送系統、聯合用藥)研發需求的新模型的探索。





[1] Guohua An. Pharmacokinetics and Pharmacodynamics of GalNAc-Conjugated siRNAs. The Journal of Clinical Pharmacology. 2024, 64(1) 45–57
[2] Jae Yoon Jeon, Vivaswath S. Ayyar. Amitava Mitra. Pharmacokinetic and Pharmacodynamic Modeling of siRNA Therapeutics – a Minireview. Pharmaceutical Research (2022) 39:1749–1759
[3] Steven F. Dowdy. Endosomal escape of RNA therapeutics: How do we solve this rate-limiting problem? RNA. 2023 Apr; 29(4): 396–401.
[4] MULTI-DISCIPLINE REVIEW of Givosiran.
https://www.accessdata.fda.gov/drugsatfda_docs/nda/2019/212194Orig1s000MultidisciplineR.pdf
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容
