
2023-08-17 00:00:00來源:陶術瀏覽量:207
Nature重磅 | 誘導癌細胞凋亡新技術,或對多數癌癥有效!
?
癌細胞獲得基因突變后,會對數千個基因的表達進行重新編程,從而促進細胞快速生長,并阻斷正常的細胞凋亡途徑。盡管細胞凋亡被阻礙,但該通路本身并未消失。那么,如果我們能重新打開癌細胞凋亡通路的開關,是不是就可以借此對抗癌癥呢?
?
以這個疑問為出發點,斯坦福大學的科學家對促癌蛋白BCL6進行了深入研究,最終找到了一種能夠誘導癌細胞凋亡的方法。他們發現一種名為轉錄/表觀遺傳 CIP(TCIP)的新型分子,能夠調控癌細胞內的癌癥生長基因表達,從而激活細胞凋亡途徑。這種方法可能對大多數的癌癥類型產生積極影響。有關這一發現的詳細內容已以?Rewiring cancer drivers to activate apoptosis?為題發表于?Nature?期刊。
?
?
BCL6 是一種轉錄因子,可直接抑制編碼細胞周期抑制因子的基因和參與細胞凋亡蛋白質的基因。然而,在某些類型的 B 細胞淋巴瘤中,BCL6 的表達被異常激活或過度表達,從而促進癌細胞的增殖、生存和侵襲。
?
?
傳統觀念認為,促癌轉錄因子是無法通過藥物靶向的,那么這項研究是如何將 BCL6 轉化為轉錄激活因子的呢?
?
在這項研究中,作者采用了一種稱為?化學誘導臨近(chemical inducers of proximity, CIP)的技術。簡單來說,CIP 是一種利用小分子將兩個蛋白質靠近,以實現特定生物學效應的方法。
一個經典的 CIP 案例是 PROTAC。正如我們所知,蛋白質降解的自然過程中包括一步叫做泛素化的階段,這一過程由一個適配蛋白介導,適配蛋白同時與目標蛋白和催化泛素化的酶結合,將它們緊密靠近。這種交互過程已被用于設計被稱為 PROTAC 的小分子藥物,這些藥物模仿適配蛋白的功能,使得特定蛋白質被有針對性地降解,以實現治療效果。
?
與 PROTAC 類似,在這項研究中,科研人員合成了一種?雙頭分子,其中一端與 BCL6 的結合目標結合,另一端與轉錄激活因子 BRD4 結合。這一創新性的化合物形成了一個?三元復合物,與 BRD4 和 BCL6 一同作用,使得 BRD4 能夠激活被 BCL6 沉默的基因。科學家們將這一化合物命名為 TCIP(Transcriptional/Epigenetic Chemical Inducer of Proximity)。
?
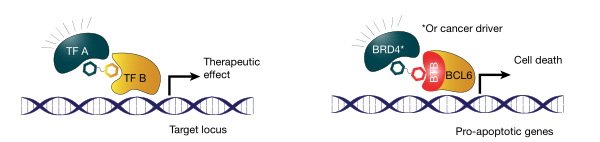
▲TCIP分子的設計
?
新型抗癌藥物——TCIP1
?
接下來,研究團隊選擇了TCIP中功能最強的分子——TCIP1,并將其應用于彌漫性大 B 細胞淋巴瘤(DLBCL)的治療。
在實驗中,TCIP1 分子表現出快速、有效地殺傷 DLBCL 細胞的能力,包括對于化療耐藥的 DLBCL 細胞系 KARPAS422 的殺傷作用。在 KARPAS422 細胞系中,TCIP1 分子的半數有效濃度(EC50)為 1.3 nM,僅在 72 小時內即可使 50% 的腫瘤細胞死亡。
?
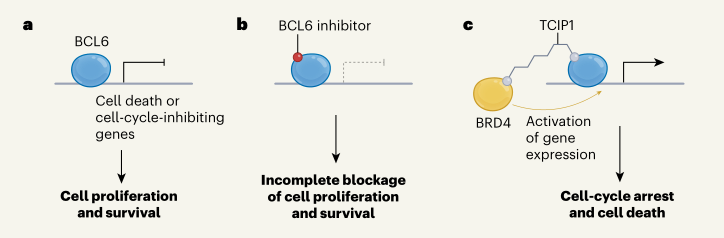
▲TCIP1有效地殺死表達BCL6的癌細胞
?
這是由于 TCIP1 能夠與 BCL6 的 BTB 結構域結合,從而抑制其與核受體共抑制因子(NCOR)、BCL6 共抑制因子(BCOR)以及視黃酸和甲狀腺激素受體的沉默介導因子(SMRT)的相互作用。這一作用使得一系列 BCL6 的靶基因能夠表達,包括與促進凋亡、細胞周期阻滯以及 DNA 損傷應答有關的基因,如 TP53。通過這種方式,轉錄調控網絡被重新構建,進而激活了細胞凋亡途徑,從而有效地抑制了癌細胞的增殖、生存、侵襲和轉移。
此外,其他表達 BCL6 的 DLBCL 細胞系同樣能夠被 TCIP1 分子迅速、有效地消滅。與此對比,僅使用 BRD4 或 BCL6 抑制劑(JQ1或BI3812)的細胞殺傷效果較弱,這表明 TCIP1 分子的選擇性殺傷效應不僅僅是將兩種抑制劑合并到細胞內的簡單疊加。
與此同時,研究團隊還合成了負對照化合物 Neg1 和 Neg2,以驗證 TCIP1 分子的特異性作用。結果顯示,這兩種化合物與 BRD4 或 BCL6 的結合能力均受到削弱,因此無法有效地殺傷 DLBCL 細胞。這些實驗結果強有力地證明了 TCIP1 分子的選擇性殺傷作用,并且?其作用機制需要 BRD4、BCL6 和 TCIP1 三者的三元復合物的共同參與。
?
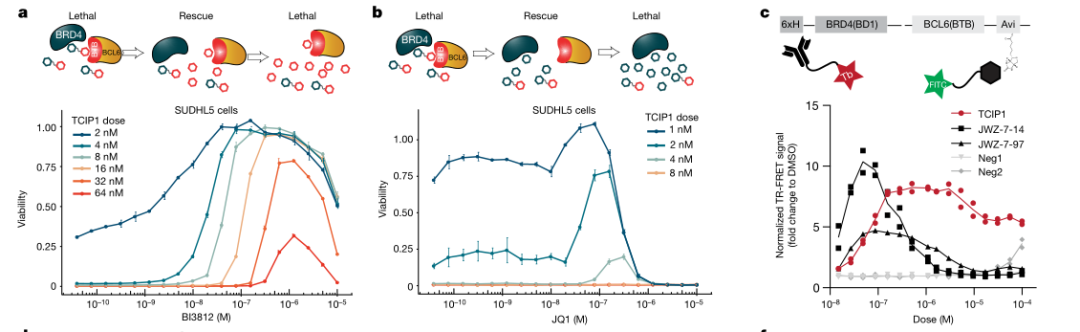
▲TCIP1通過誘導三元復合物形成發揮功能
?
此外,通過實驗觀察,科研人員發現 TCIP1 分子誘導 DLBCL 細胞的凋亡不僅限于特定細胞周期階段,而是在?整個細胞周期中均可發生。他們還鑒定了參與 TCIP1 分子誘導細胞凋亡的直接靶標基因。
通過向 KARPAS422 細胞中添加 10 nM 的 TCIP1 分子,隨后分別在不同時間點進行 RNA 測序,科研人員?鑒定了大約 140 個被 TCIP1 分子誘導的基因,其中包括 BCL6 抑制的靶標基因,如 BCL2L11、BIM、PMAIP1、FOXO3 和 BCL6 等。并且,TCIP1 還下調了 MYC(編碼轉錄因子的促腫瘤基因)及其多個轉錄靶標的表達。這些結果表明,TCIP1 分子能夠直接調節多個基因的表達,從而影響細胞的生長和凋亡。
?
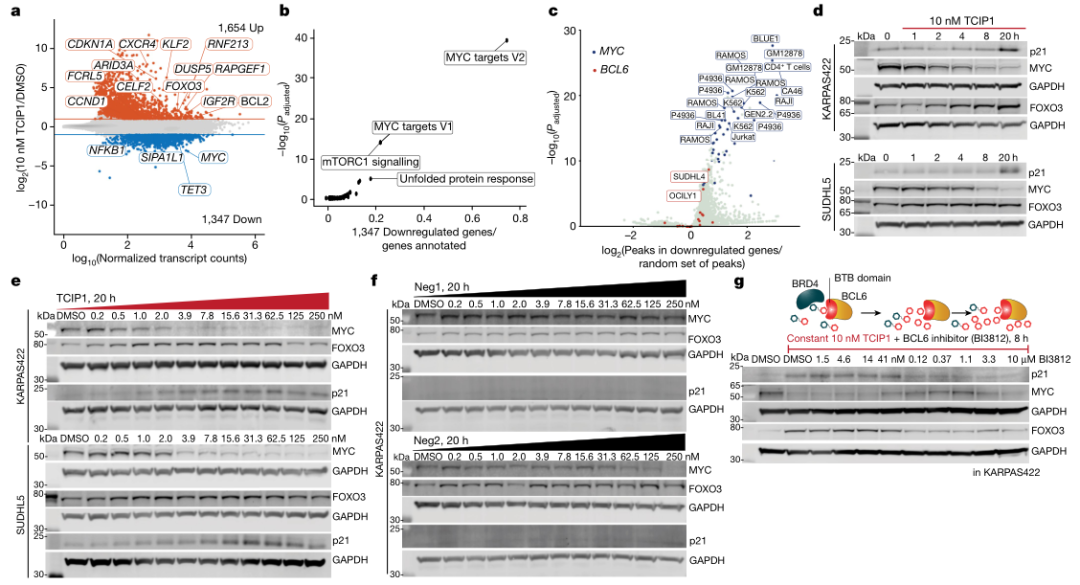
▲TCIP1在激活促凋亡基因的同時抑制MYC及其靶點
?
總結
?
綜上,該研究介紹了一種新的治療癌癥的策略,即利用TCIP分子來激活細胞死亡途徑,從而抑制癌細胞的增殖和生存。研究人員設計了一種雙頭分子化合物TCIP1,其中一個結合BCL6的分子與另一個結合BRD4的分子相連。這種化合物形成了一個復合物,與基因組中BCL6結合位點上的BRD4和BCL6一起作用,迅速激活轉錄延伸和相關靶向基因的表達。通過這種方式,TCIP1可以殺死表達BCL6的DLBCL細胞。
?
作者還討論了TCIP策略的普適性,認為該策略除了治療DLBCL外,還可以用于治療多種表達BCL6的腫瘤。總之,該研究為開發新的癌癥治療策略提供了新思路和方法。
?
參考資料:
[1] Gourisankar S, Krokhotin A, Ji W, et al. Rewiring cancer drivers to activate apoptosis. Nature. 2023;620(7973):417-425. doi:10.1038/s41586-023-06348-2 [2] Phelan JD, Staudt LM. Double-headed molecule activates cell-death pathways in cancer cells. Nature. 2023;620(7973):285-286. doi:10.1038/d41586-023-02213-4
?