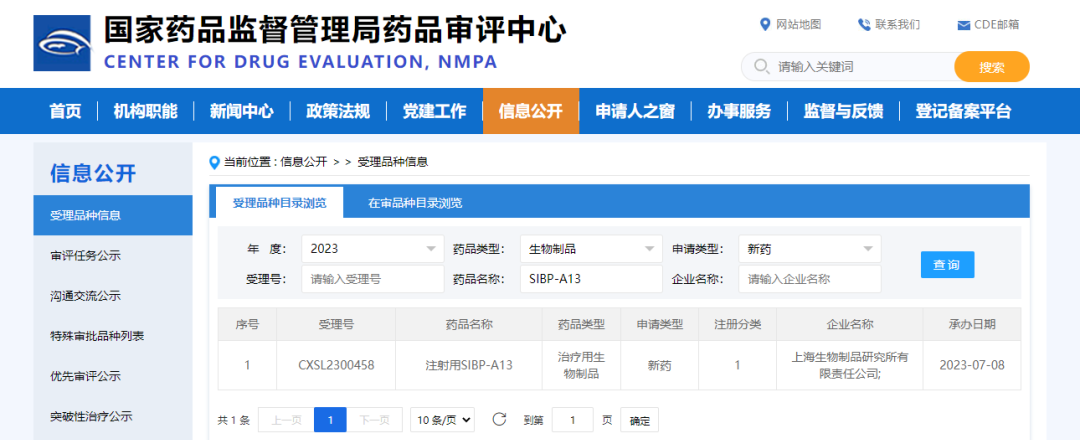
7月7日,國藥集團中國生物上海生物制品研究所自主研發(fā)的創(chuàng)新型抗體偶聯(lián)藥物(ADC)SIBP-A13臨床試驗申請獲國家藥品監(jiān)督管理局藥品審評中心(CDE)正式受理。這是中國生物研發(fā)的首個創(chuàng)新型抗體偶聯(lián)藥物,標志著上海生物制品研究所抗體偶聯(lián)藥物研發(fā)已從技術(shù)平臺創(chuàng)新轉(zhuǎn)入了臨床開發(fā)的新階段,具有重要里程碑意義。SIBP-A13是上海生物制品研究所基于國內(nèi)領先的第3代ADC技術(shù)研發(fā)的靶向HER3 ADC新藥,具有連接子可裂解、載荷活性強、抗腫瘤“旁觀者效應”等藥物優(yōu)勢。SIBP-A13具有完全自主知識產(chǎn)權(quán),其中抗HER3單抗分子、偶聯(lián)技術(shù)連接子均為自主研發(fā),臨床前數(shù)據(jù)顯示其可有效抑制多種腫瘤生長,具有良好耐受性,臨床上擬用于晚期惡性實體瘤治療。SIBP-A13在抗體基礎上偶聯(lián)小分子細胞毒性藥物,兼具了抗體的靶向性和細胞毒性藥物的殺傷性。其可借助抗體靶向作用與腫瘤細胞表面的靶抗原結(jié)合,而偶聯(lián)小分子藥物則經(jīng)內(nèi)吞效應進入腫瘤細胞并釋放,從而精準殺傷腫瘤細胞以及腫瘤周圍病變細胞。聲明:本文系藥方舟轉(zhuǎn)載內(nèi)容,版權(quán)歸原作者所有,轉(zhuǎn)載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內(nèi)容、版權(quán)和其它問題,請與本網(wǎng)站留言聯(lián)系,我們將在第一時間刪除內(nèi)容