
2023-05-06 16:30:40來源:醫藥地理瀏覽量:462
4月25日,Biogen/lonis聯合宣布FDA已同意加速批準用于治療超氧化物歧化酶1(SOD1)突變所致肌萎縮側索硬化(ALS)的反義寡核苷酸療法Tofersen上市,這是首款針對ALS的基因靶向療法。

圖1:Biogen官網公告稱FDA加速批準治療ALS的Tofersen上市
肌萎縮側索硬化癥(ALS)是一種病因未明、主要累及大腦皮質、腦干和脊髓運動神經元的神經系統變性疾病。其局限性分型包括進行性球麻痹(PBP),連枷臂、腿,進行性肌萎縮(PMA),原發性側索硬化(PLS)。我國通常將肌萎縮側索硬化和運動神經元病混用。此前國際上所統計的患病率約為4-10萬人,僅美國ALS患者就近3萬人。目前,ALS的致病原因還不清楚,只有5%-10%的患者有明確的遺傳因素。SOD1-ALS是ALS的一種罕見遺傳性形式,僅占全球約16.8萬ALS病例的2%。
Tofersen是一種用于治療SOD1-ALS的反義寡核苷酸藥物。Tofersen可與編碼SOD1的mRNA結合,使其被核糖核酸酶降解,從而減少SOD1蛋白的產生。Biogen根據合作開發和許可協議從Ionis獲得了Tofersen的許可。
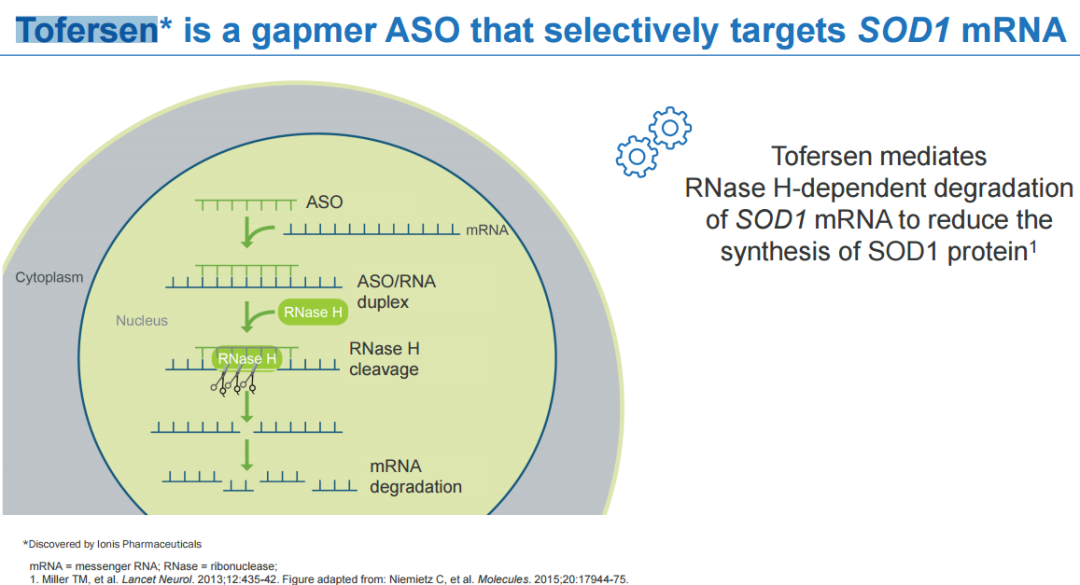
圖2:Tofersen藥物作用原理
在一項為期28周的隨機、雙盲、安慰劑對照VALOR臨床研究中,對108名23至78歲因SOD1基因突變引起ALS的患者以2:1的比例隨機接受Tofersen 100mg(n =72)或安慰劑(n = 36)治療持續24周以評估了Tofersen的療效,允許患者同時使用利魯唑和/或依達拉奉,基線時62%的患者服用利魯唑,8%的患者服用依達拉奉。根據臨床試驗研究結果顯示,接受Tofersen治療的患者人群在臨床肌萎縮側索硬化功能評定量表(ALSFRS-R)相較基線下降較少(p=0.97),該研究不具有統計學意義。
雖然在完成VALOR臨床試驗并參加開放標簽擴展(OLE)研究的52周參與者中期分析中,Tofersen的早期開始與臨床功能(ALSFRS-R)、呼吸強度(預測的緩慢肺活量百分比)和肌肉力量(手持式測力megascore)下降沒有統計學意義。但在生物標志物研究中,Tofersen可顯著降低患者體內SOD1蛋白水平,且降低了與神經軸突損傷相關的神經絲輕鏈(NfL)的水平。神經絲輕鏈蛋白(NfL)是神經絲蛋白中的重要組成部分,當神經元或其軸突受損時,大量NfL會被釋放到血漿和腦脊液中。有研究表明,NfL是神經退行性標志物,可作為神經退行性疾病的替代終點。因此,Biogen基于Tofersen能夠顯著降低NfL水平,向FDA提出加速批準的申請。
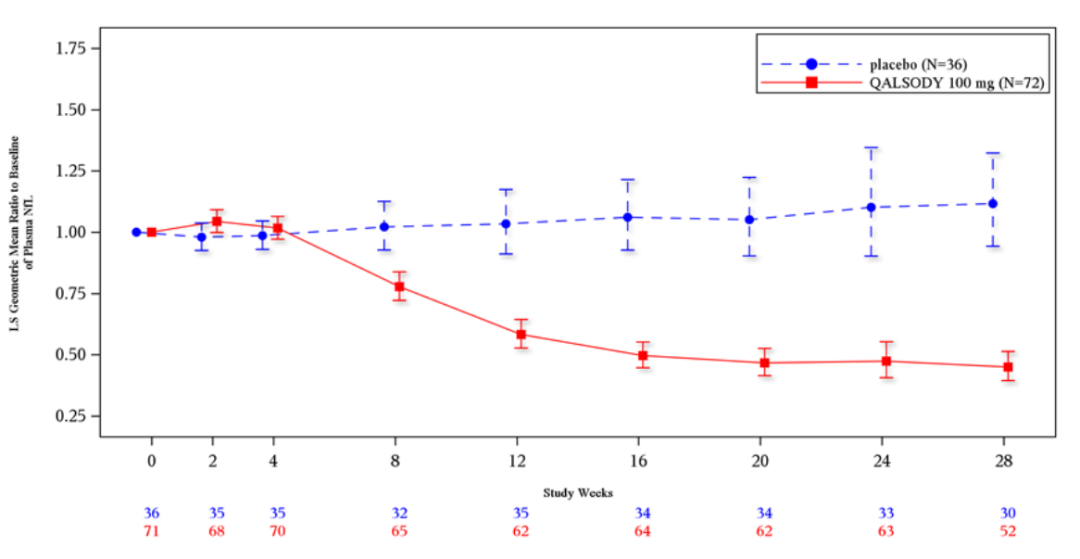
圖3:開放標簽擴展(OLE)研究相關數據
FDA指出,通過生物標志物NfL水平可以有效預測ALS患者的疾病發展,NfL水平與ASL患者的疾病進程呈現相關性,NfL水平的降低可以使ALS患者疾病進展速度減緩。因此,FDA支持將NfL水平作為預測ALS患者疾病進展速度的替代終點,這些結果發表在《新英格蘭醫學雜志》上。
據CPM新藥研發監測數據庫顯示,截至目前,在全球范圍內針對肌萎縮側索硬化癥的藥物共有4種,美國食品藥品監督管理局(FDA)批準了3種,分別為利魯唑、依達拉奉、和復方苯丁酸鈉+牛磺熊去氧膽酸。韓國食品藥品安全部(MFDS)批準了倫邁托賽(lenzumestrocel)上市。

圖4:全球目前已上市用于治療ALS的藥品
利魯唑(riluzole)是賽諾菲(Sanofi)公司開發的藥物,1996年美國FDA批準上市,是第一個獲美國FDA和歐盟批準用于治療ALS的藥物。利魯唑屬于苯并噻唑類化合物,具有明確的神經保護藥理作用。它的主要作用是抑制多種受體和離子通道介導的谷氨酸突觸傳導和神經元超興奮性,提高神經營養因子的表達量,保護神經元免受興奮毒性損傷,保護神經元的存活,從而可以改善ALS患者的生活質量。利魯唑以片劑形式給藥,可能導致頭暈、胃腸道疾病和肝功能改變等副作用。
依達拉奉(edaravone)是一種自由基清除劑,由2001年日本田邊三菱制藥公司研制上市,治療腦卒中。有研究認為,依達拉奉可清除自由基并防止腦細胞(血管內皮細胞/神經細胞)出現氧化損傷,從而ALS的疾病進展。該藥用于治療ALS適應癥在日本(2015年)以商品名Radicut獲準上市,在美國(2017年)和加拿大(2020年)以商品名Radicava獲準上市。
復方苯丁酸鈉+牛磺熊去氧膽酸由美國馬薩諸塞州總醫院Sabrina Paganoni團隊研究,并于2020年9月3日在《新英格蘭醫學雜志》發表相關成果。在后續的臨床實驗中,該療法被證明安全、有效且耐受良好,可以通過阻斷源自線粒體和內質網的應激通路來防止神經細胞死亡。
倫邁托賽(lenzumestrocel)是世界上第一個基于干細胞治療ALS的療法,在2014年韓國食品藥品安全部批準該藥上市。倫邁托賽選取自體骨髓來源的間充質干細胞(MSCs),與患者的腦脊液混合,并通過鞘內注射進行給藥。
總的來看,Biogen在ALS治療領域中仍然面臨較大的壓力。就在宣布Tofersen被納入加速批準隊列的的同一天,Biogen公布了2023Q1的財務數據:第一季度收入24.63億美元,同比下降3%。
此前,業績的壓力已經迫使Biogen取消某些卒中、基因治療和眼科項目,將資源集中于阿爾茨海默病(AD)項目。Biogen成立于2003年,核心管線覆蓋包括肌萎縮側索硬化癥(ALS)、多發性硬化(MS)、阿爾茨海默病(AD)在內的多種中樞神經系統(CNS)疾病治療藥物。但由于大部分CNS疾病發病機制不明確,導致試驗設計困難。雖然這次Tofersen的加速批準讓Biogen看到了希望,但由于該藥市場潛力較小,對Biogen的業務幫助也不大,未來Biogen仍需要將重點放在AD項目上。