CDK4/6全稱為細胞周期蛋白依賴性激酶4和6,是驅動細胞分裂的關鍵調節因子。研究發現作為細胞周期的關鍵調節因子,CDK4/6能夠觸發細胞周期從生長期(G1期)向DNA復制期(S1期)轉變,導致癌細胞分裂周期失控,無限增殖。自2015年2月Ibrance(哌柏西利)首次獲批以來,目前全球共有5款CDK4/6靶向新藥上市,除了達爾西利僅在中國獲批上市未披露銷售數據外,其余4款全球市場總規模基于最新財報數據已持續增長至近90億美元。
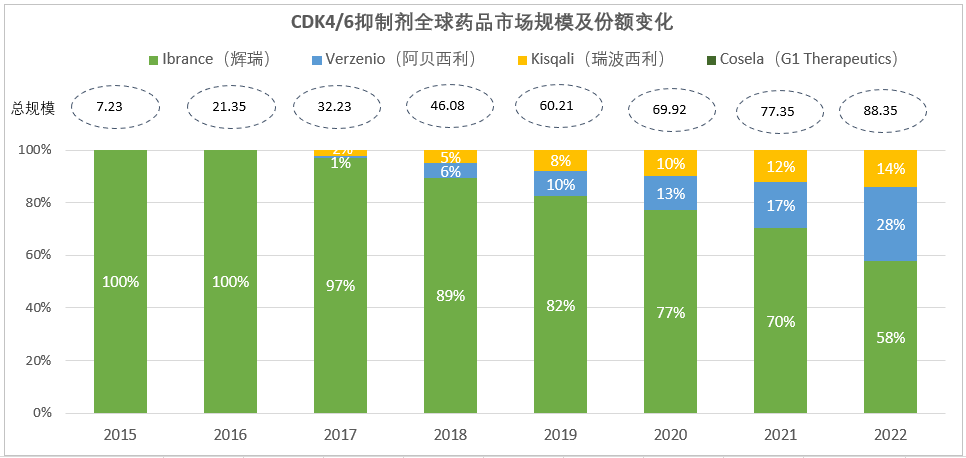
注:1)數據來源于公司財報,市場規模按億美元計;2)Cosela在2021年銷售收入0.11億美元,2022年銷售額尚未披露,占比預計低于1%
除了G1/先聲藥業開發的Trilaciclib(曲拉西利)獲批化療引起的骨髓抑制適應癥之外,當前上市的CDK4/6抑制劑適應癥主要是乳腺癌,這也是人數最多的癌癥患者群體。根據WHO國際癌癥研究機構(IARC)發布的全球最新癌癥數據,2020年全球乳腺癌新增人數達226萬,首次超過肺癌(221萬),成為全球第一大癌癥。
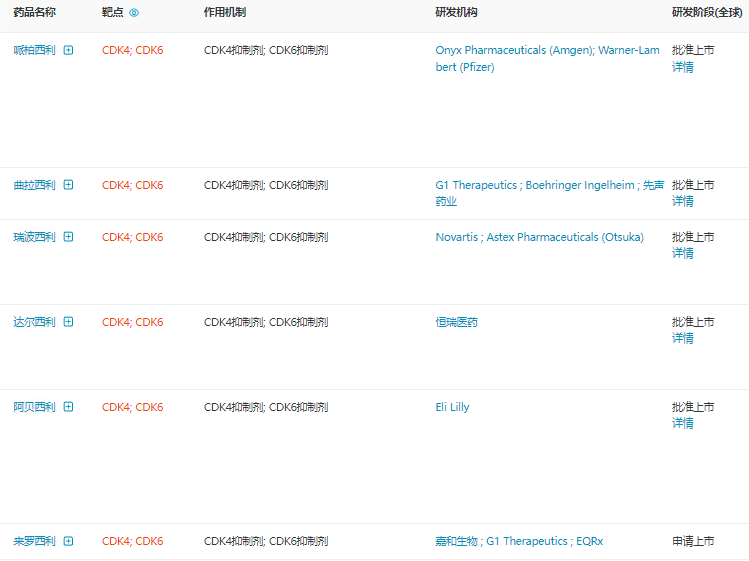
就在3月28日,CDE官網公示,G1 Therapeutics與嘉和生物共同遞交了CDK4/6抑制劑鹽酸來羅西利片(lerociclib,GB491)的上市申請并獲得受理,筆者推測適應依然為乳腺癌。并且同一天(3月28日),上海醫藥披露其研發的CDK4/6抑制劑SPH4336用于脂肪肉瘤適應癥獲得FDA孤兒藥資格認定(Orphan-drug Designation)(申請編號:DRU-2022-9305)。公告顯示,SPH4336是一種新型高選擇性口服CDK4/6抑制劑,具有廣譜的抗腫瘤作用,正在中國開展針對晚期實體瘤的I期臨床試驗,且正在美國開展針對局部晚期或轉移性脂肪肉瘤的II期臨床試驗。截止目前,該項目在全球已累計投入研發費用約人民幣12,589萬元。

根據《孤兒藥法案》,FDA的孤兒藥認定能夠加快推進臨床試驗及上市注冊的進度。同時可享受一定的政策支持,包括但不限于臨床試驗費用的稅收抵免、免除 新藥申請費、產品獲批后將享受7年的市場獨占權。軟組織肉瘤是罕見的具有50多種組織學亞型的惡性腫瘤。軟組織肉瘤的年發病率略高于骨肉瘤,每年約有2-5/10萬人,仍然是一種罕見的疾病。在各種軟組織肉瘤中,脂肪肉瘤(LS)是最為常見的,但整體發病率極低,每年約有1-4/百萬人發病。脂肪肉瘤可以在任何年齡發生,但最常見的發病年齡是50-70歲。脂肪肉瘤發病男女性別差異不大。脂肪肉瘤起源于有向脂肪組織分化傾向的原始間充質細胞,好發于深部軟組織,最常見的部位是四肢和軀干的深部軟組織,特別是在股骨、髂骨和肩胛骨附近。
一些研究表明,與脂肪肉瘤有關的風險因素包括肥胖、糖尿病、遺傳因素、某些疾病的治療方法等。脂肪肉瘤的預后較差,其5年生存率大約為50%左右,但具體預后取決于病情的嚴重程度、患者年齡、腫瘤部位等因素。
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容



