
2023-03-14 12:04:50來源:醫藥觀瀾瀏覽量:322

公開資料顯示,來凱醫藥成立于2016年,致力于為全球癌癥及肝纖維化患者帶來突破性的療法。該公司核心管理團隊包括董事長兼首席執行官(CEO)呂向陽博士,首席醫學官岳勇博士和首席科學官顧祥巨博士。成立以來,該公司已先后完成多輪融資,包括2022年5月完成的6100萬美元D輪融資。
在開展自主研發的同時,來凱醫藥還先后與諾華(Novartis)達成多次合作,獲得開發、制造及商業化LAE002、LAE001、LAE005及LAE003的全球獨家權益。下面,我們將節選來凱醫藥部分在研創新藥項目作介紹。
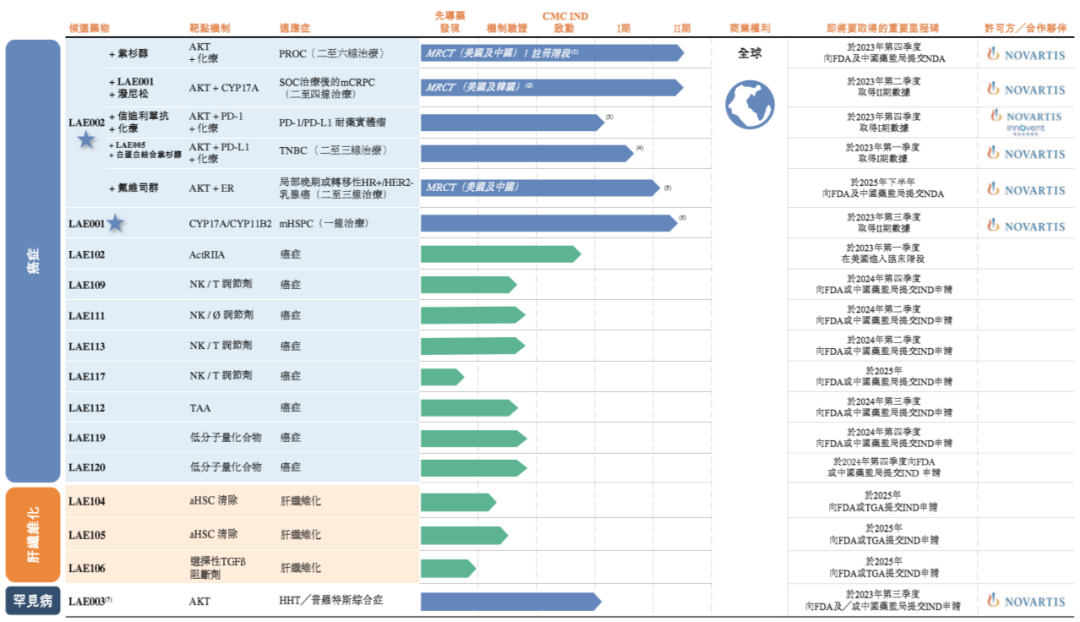
▲來凱醫藥部分產品管線(截圖來源:參考資料[1])
LAE002(afuresertib)是一種三磷酸腺苷(ATP)競爭性AKT抑制劑,擬用于治療卵巢癌、前列腺癌、乳腺癌及PD-1/PD-L1抑制劑耐藥實體瘤。AKT通路活性的上調與許多癌癥中的標準療法(SOC)耐藥性有關,AKT抑制劑已在眾多臨床研究中證實其改善耐藥性的能力。來凱醫藥已在美國及中國啟動了針對LAE002聯合紫杉醇治療鉑耐藥卵巢癌(PROC)的全球國際多中心2期注冊試驗。該公司的目標是于2023年第四季度向美國FDA及中國國家藥監局(NMPA)提交NDA。
此外,來凱醫藥還在開展LAE002的多項臨床試驗。其中包括針對轉移性去勢抵抗型前列腺癌(mCRPC)的2期國際多中心臨床試驗、針對三陰性乳腺癌(TNBC)的1/2期臨床試驗、針對HR+/HER2-局部晚期或轉移性乳腺癌的1b/3期臨床試驗、針對PD-1/PD-L1抑制劑耐藥性實體瘤的1/2期臨床試驗等。
LAE001是一款雄激素合成抑制劑,可同時抑制細胞色素P450家族17亞族A成員1(CYP17A1)及細胞色素P450家族11亞族B成員2(CYP11B2),擬用于治療前列腺癌。已完成的1期研究顯示出在不使用潑尼松下,LAE001單藥療法的安全性、初步抗腫瘤功效及對轉移性去勢抵抗型前列腺癌(mCRPC)患者的潛在臨床益處。目前,來凱醫藥正進行LAE001單藥療法用于治療mCRPC的2期臨床試驗。該公司還計劃于2023年第四季度在中國及美國開始轉移性激素敏感型前列腺癌(mHSPC)的3期國際多中心注冊試驗。
LAE005是一種高親和力、阻斷配體的人源化抗PD-L1 IgG4抗體。在臨床前研究及臨床研究中,該產品證實了其對PD-L1的結合親和力并具有抗腫瘤活性。目前,來凱醫藥正評估LAE002與LAE005聯合療法對三陰性乳腺癌患者的治療潛力。該公司計劃于2024年第一季度在中國啟動該產品的2期研究。
LAE003是一種ATP競爭性AKT強效抑制劑。在臨床前研究中,該產品對AKT1、AKT2和AKT3表現出有效性及選擇性。目前,LAE003腫瘤適應癥已處于臨床階段,來凱醫藥正在將其重新用于治療罕見病——遺傳性出血性毛細血管擴張癥(HHT)和普羅特斯綜合癥。
LAE102是來凱醫藥自主研發的一款治療癌癥的候選藥物。這是一種強效及選擇性的activin受體IIA型(ActRIIA)單克隆抗體,在臨床前動物模型中顯示出抗腫瘤活性及增加荷瘤動物體重的能力。
LAE105是來凱醫藥自主研發的一款治療肝纖維化的候選藥物,針對活化肝星狀細胞(aHSC),并已進入機制驗證臨床前研究。
此外,來凱醫藥在研管線還有多款自主研發的針對腫瘤和肝纖維化的在研管線。限于篇幅,此處不再一一介紹。
[1]來凱醫藥招股書. Retrieved Mar 13 , 2023. From https://www1.hkexnews.hk/app/sehk/2023/105223/documents/sehk23031301153_c.pdf
[2]來凱醫藥官網. From https://www.laekna.com/about#aboutlaekna
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容