
2023-03-06 10:53:44來源:醫藥觀瀾瀏覽量:391
中國國家藥監局藥品審評中心(CDE)官網公示,海雁醫藥申報的1類新藥YZJ-5053片已經獲得臨床試驗默示許可,擬定適應癥為:經標準治療后或在治療中發生腫瘤進展,或目前無標準治療可用、已不適合接受根治性治療的晚期/轉移性實體瘤。公開資料顯示,YZJ-5053是一款雙腺苷(A2aR/A2bR)靶點受體抑制劑,此前已于2022年8月在美國獲批臨床。
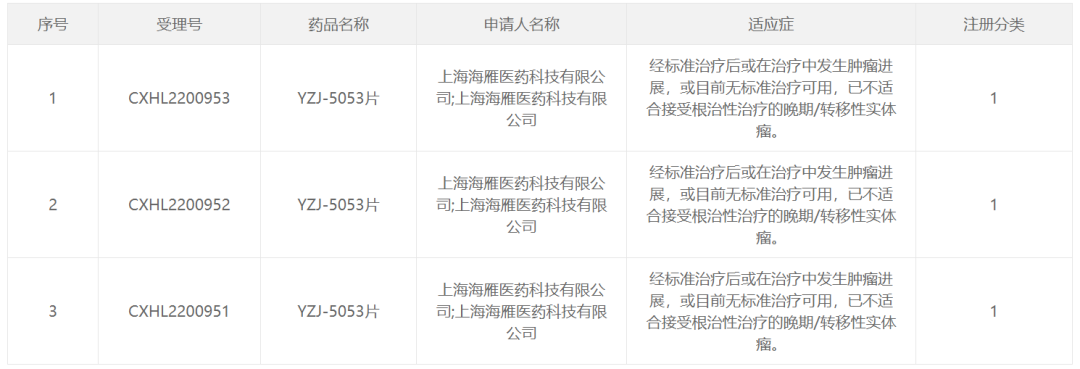
截圖來源:CDE官網
近年來免疫治療在晚期癌癥的治療中獲得了突破性成功,但是由于腫瘤微環境中多種代償性的免疫抑制機制的存在,導致免疫治療的響應率欠佳。公開資料顯示,腺苷是腫瘤內部產生的一種較為強大的免疫抑制物質,是癌細胞快速周轉的結果,并通常與某些抗腫瘤干預措施有關,如化療和放療。A2a/A2b受體表達于免疫細胞表面,腺苷通過直接與腫瘤浸潤免疫細胞上的A2a受體和A2b受體相互作用,從而介導免疫抑制作用。開發腺苷A2a/A2b受體抑制劑有望解除腺苷介導的免疫抑制作用。

據海雁醫藥早先新聞稿介紹,YZJ-5053正是一種具有高活性,高選擇性,低毒性的雙腺苷(A2aR/A2bR)靶點受體抑制劑。研究顯示該產品與PD-1/PD-L1抑制劑類藥物聯用具有協同增效作用,在多個小鼠腫瘤模型中觀察到免疫聯合治療作用下的腫瘤消退現象。
公開資料顯示,海雁醫藥成立于2011年5月,是揚子江藥業的全資子公司和創新藥物研發基地。該公司以神經系統、腫瘤、免疫系統、消化道疾病等為主要研發方向,目前在研化學1類創新藥物20余項,多個項目處于臨床階段,其中2個項目處于臨床3期階段。
參考文獻:
[1]中國國家藥監局藥品審評中心(CDE)官網 . Retrieved Mar 3, 2023, from https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c
[2]上海海雁Ⅰ類創新藥YZJ-5053片臨床試驗申請獲FDA正式批準. Retrieved Aug 29, 2022, From https://mp.weixin.qq.com/s/qLMG0Wuslnf_HU0rdW1cbQ
[3]揚子江藥業官網 .From http://n.yangzijiang.com/html/yjkf_detail01.html
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容