
2023-02-21 11:45:38來源:藥智網瀏覽量:190
近日,宜明細胞自主馴化的懸浮293XSTM細胞庫完成了向美國FDA的DMF備案,并已收到確認函,備案號為DMF 28844。
293XSTM細胞株適用于多種AAV血清型的大規模生產,已獲得中國國家知識產權局頒發的發明專利證書。未來,宜明細胞客戶的AAV項目在進行IND申報時,可直接引用相應的DMF備案號,極大地縮短產品審查和評估時間,簡化IND申報資料包,從而加速相關藥品的項目申報進程。

宜明細胞懸浮293XSTM細胞庫DMF備案確認函
圖片來源:宜明細胞官微
在基于“三質粒瞬轉法”的AAV生產平臺中,可放大的、穩定的細胞株是核心組分之一。宜明細胞的293XSTM細胞庫:
高密度,培養密度可達1E7 cells/ml
可放大,可實現50L-200L-500L-2000L規模細胞培養
高產率,AAV產率可超過1E14VG/L
安全,無輔助病毒、 無動物來源組分
提供完善的文件證明,細胞庫生產符合GMP標準,完全滿足中美雙報的要求
自主馴化可授權,已獲得中國國家知識產權局頒發的發明專利證書
完成了向美國FDA的DMF備案,極大地縮短產品審查和評估時間
2022年,由宜明細胞生產且獲批IND的三款AAV基因藥物所使用的都是293XSTM細胞株*
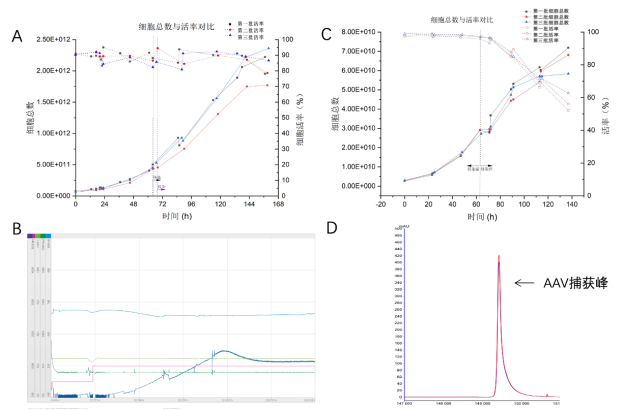
圖片來源:宜明細胞官微
293XSTM的部分數據(數據源自宜明細胞)|A:200LAAV生產體系,3批細胞總數與活率對比數據 ;B:200L生物反應器發酵曲線;C:Wave 25LAAV生產體系,3批細胞總數與活率對比數據;D:200L AAV生產體系,經第一步親和層析捕獲后,空殼率僅為56%。
*:與宜明細胞合作的三款獲批NMPA IND的AAV項目分別是天澤云泰的“VGR-R01”和“VGB-R04 ”以及朗昇生物的“LX101”。
目前,宜明細胞已有三項自主研發品種完成在美國FDA的DMF備案,詳見下表:
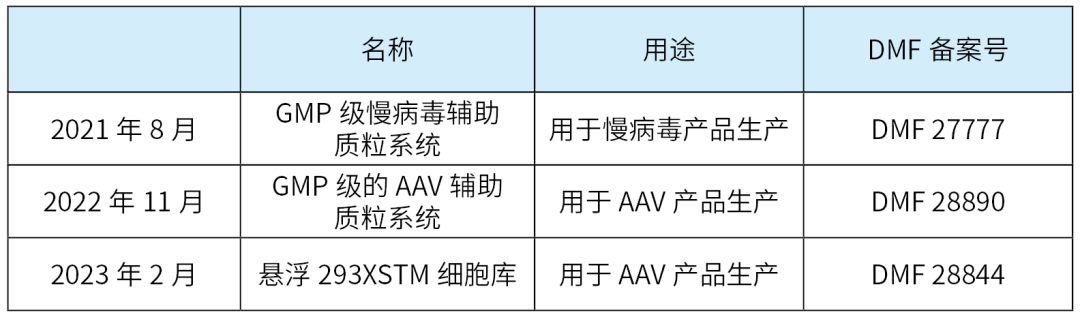
圖片來源:宜明細胞官微
DMF是指原料供應商遞交給FDA的藥物存檔文件,包含藥物產品在生產、操作、包裝和儲存過程中用到的設施、操作流程、原料等保密細節信息。根據美國聯邦食品、藥品和化妝品法等規定,藥品在上市之前必須向FDA提出相關的申請(如臨床研究申請(IND)、新藥注冊(NDA)和生物制品許可證申請(BLA)等),并需要提供該藥物在安全性、有效性和質量三方面的全部信息,其中還涉及到原料藥以及輔料等相關技術內容。這些信息不僅繁冗復雜,而且涉及保密需求。DMF(Durg Master Files, 藥品主文件)體系于是應需而生。
宜明細胞將以上信息以DMF文件的形式在FDA備案并獲得相應產品的DMF備案號,為宜明細胞客戶在基于慢病毒以及AAV載體項目的申報中節約了審批成本、提高了審批效率、并且縮短了注冊周期。
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容