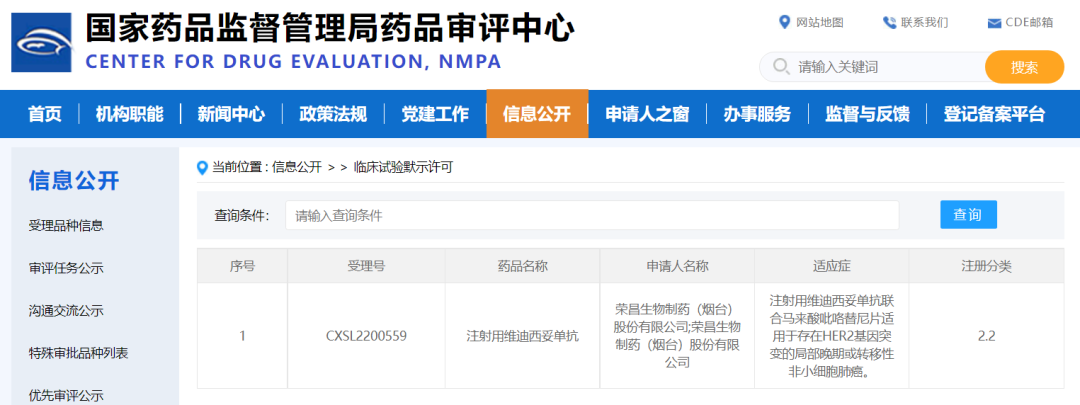
2月14日,榮昌生物宣布:注射用維迪西妥單抗聯合馬來酸吡咯替尼片治療存在HER2基因突變的局部晚期或轉移性非小細胞肺癌患者的安全性、有效性及藥代動力學特征的開放、單中心Ib/II期臨床研究正式獲得國家藥監局藥審中心批準。
該項研究的主要目的是評價維迪西妥單抗聯合馬來酸吡咯替尼在存在HER2基因突變的局部晚期或轉移性非小細胞肺癌患者中的安全性和耐受性,確定維迪西妥單抗聯合吡咯替尼的劑量限制性毒性、最大耐受劑量/推薦聯合劑量。非小細胞肺癌是起源于支氣管黏膜、支氣管腺體和肺泡上皮的一類肺惡性腫瘤,是世界上最常見的惡性腫瘤之一,已成為我國城市人口惡性腫瘤死亡原因的第1位。非小細胞肺癌約占所有肺癌的80%,約75%的患者發現時已處于中晚期,5年生存率很低。HER2突變可促進腫瘤細胞的增殖、存活、侵襲和轉移,攜帶HER2基因激活突變的非小細胞肺癌患者預后不良,存在巨大未被滿足的臨床需求。維迪西妥單抗(商品名:愛地希?)是由榮昌生物自主研發的中國首個原創抗體偶聯(ADC)藥物,以腫瘤細胞表面的HER2蛋白為靶點,能精準識別和殺傷腫瘤細胞,在治療尿路上皮癌等腫瘤的臨床試驗中取得了卓越的臨床數據,是我國首個被美國FDA、中國藥監局授予突破性療法的ADC藥物。2021年,維迪西妥單抗胃癌適應癥、尿路上皮癌適應癥先后獲中國藥監局批準上市銷售,目前均已獲批進入國家醫保藥品目錄。該藥用于治療尿路上皮癌的全球多中心關鍵性Ⅱ期臨床試驗正在快速推進。聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容