
2022-12-05 09:46:18來源:醫藥魔方瀏覽量:227
新冠病毒的出現對全人類的生活、工作造成巨大影響,也逐漸引發大家對這種肉眼見不到的微生物威力的認識,以及當下及未來如何應對這類感染性疾病的思考。
事實上,在人類歷史長河中,既出現過像新冠這種突然爆發,通過空氣快速傳播的大規模流感病毒,也存在很多傳播速度不快,但致命性極強的感染性病毒。比如,埃博拉病毒、艾滋病毒、狂犬病毒等。
回顧很多古老疾病,人類至今仍有許多還未征服,狂犬病就是其中一種。作為幾乎100%致死的疾病,提及狂犬病往往令人“談犬色變”,但它又是可預防的。今天,我們就和大家聊一聊現代醫學如何一步一步“壓制”狂犬病毒實現狂犬病可預防。
疫苗——狂犬病預防的第一道防線
狂犬病(Rabies)是由狂犬病病毒(Rabies virus)感染引起的一種動物源性傳染病。當人被患狂犬病的動物咬傷,或者被抓撓或傷口、粘膜被污染時,狂犬病毒開始在被咬傷的肌肉組織中復制,然后通過運動神經元的終板和軸突侵入外周乃至整個中樞神經系統,在感染末期,心、胰腺、腎上腺和胃腸道等神經外組織也同時受累,導致患者死亡。
近年來,狂犬病報告死亡數一直位居我國法定報告傳染病前列,據國家衛健委發布的《2021年全國法定傳染病疫情概況》數據顯示,2021年我國犬病死亡150人,僅次于艾滋病、肺結核和病毒性肝炎,是我國第四大感染性疾病,給人民群眾生命健康帶來嚴重威脅。
狂犬病被記載已有四千多年歷史,古往今來的眾多科學家都投身于尋找應對狂犬病的方案。從1880年開始,巴斯德便與同僚進行狂犬病的研究。直到1885年,“微生物學之父”路易·巴斯德(Louis Pasteur)通過將發病動物的脊髓提取液反復干燥傳代減毒后制備出了第一支疫苗[1],才使得狂犬病成為了一種可預防的病毒性疾病。
1885年,該款疫苗首次用于9歲狂犬病毒感染患兒,并使他奇跡般地度過病毒潛伏期,活了下來。為了紀念巴斯德先生在研制狂犬病疫苗方面的突出貢獻,人們將其逝世紀念日——9月28日,設立為世界狂犬病日。
被動免疫——狂犬病毒預防的第二道防線
那么,是不是接種了狂犬病毒疫苗就意味著狂犬病可以100%得到預防呢?答案是否定的。
狂犬病毒暴露后預防(PEP)接種疫苗可誘導機體發生主動免疫,但是對于既往無狂犬病疫苗接種史的人群,在接種首劑疫苗后,機體免疫系統發生應答產生抗體需要7~14d的時間。對于狂犬病暴露風險高、潛伏期短的病例,僅接種疫苗可能導致免疫失敗。
因此,被動免疫成為了狂犬病PEP的重要措施之一,其機制是在第一針狂犬病疫苗注射后至機體產生足量抗體前的窗口期提供即時的免疫保護。
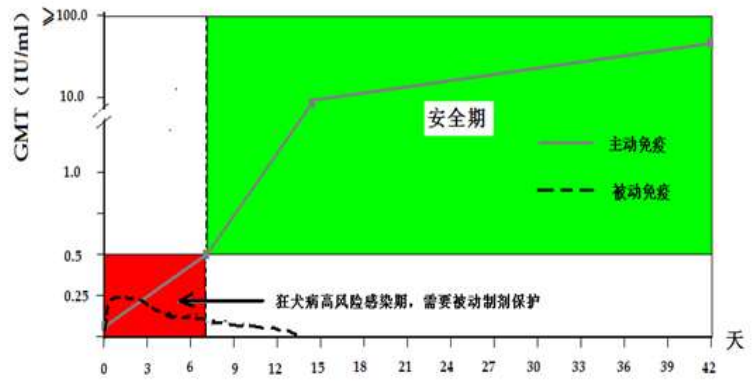
狂犬病免疫球蛋白的作用機制簡圖[2]
1954年在伊朗一起瘋狼咬傷18人的事件中,5人僅單用疫苗治療,最終3人患狂犬病死亡;而暴露程度相似的另外13人采用疫苗聯合抗血清治療,最終僅1人患病死亡。2010年我國報告的一起狂犬咬傷多人面部事件中,單純采用疫苗治療的暴露者發病死亡,而其余暴露者采用聯合被動免疫制劑治療后均存活[2]。
目前,已上市用于狂犬病預防的被動免疫制劑包括抗狂犬病馬血清(ERA)、狂犬病人免疫球蛋白(HRIG)和重組人源抗狂犬病病毒單克隆抗體(rhRIG)[3],rhRIG也就是我們平常所說的中和抗體。
雖然市場上已有HRIG和ERA被動免疫療法。不過,這兩類藥物均存在不夠完善的地方:HRIG為血液制品,來源和供應量有限,價格偏高,并有血源傳播疾病的潛在風險;而ERA在人體內半衰期較短,所需注射劑量比HRIG高,并有過敏反應甚至血清的安全性風險[4]。
中和抗體因其良好的安全性及可獲得性成為狂犬病預防中目前看來最有前景的被動免疫制劑。
中和抗體——狂犬病毒下一代被動免疫潛力之星
抗狂犬病病毒中和抗體因批間效價差異小、安全性高、可大量制備,因此有替代HRIG、ERA的潛力。另外,中和抗體另一個優勢是可快速開發制備并運用于臨床。
以新冠病毒為例,中和抗體是最先被研發出來應對疫情的武器。在新冠爆發不到一年,再生元/羅氏抗體雞尾酒療法REGEN-COV最先獲FDA緊急使用授權,成為了首個具有確證性和統計學顯著抗新冠病毒活性的治療方法[5],其獲批速度甚至跑贏了新冠mRNA疫苗。
截至目前,全球有3款抗狂犬病毒單抗獲批上市,而國內,僅華北制藥的奧木替韋單抗在今年初獲國家藥監局批準上市。現在已經進入臨床的在研產品共3款,包括智翔金泰開發的全球首創抗狂犬病毒雙特異性抗體GR1801注射液,華北制藥另一款抗狂犬病毒單抗NM57S/NC08組合制劑,以及深圳龍瑞藥業/興盟生物開發的重組人源化單抗雞尾酒療法SYN023。
進入臨床階段的抗狂犬病毒單抗
那么,既然已有單抗了,為什么還要開發“雞尾酒療法”和雙特異性抗體呢?
這主要是由狂犬病毒的性質決定的。截至2014年,已確定的狂犬病病毒株多達14種[3],不同的狂犬病病毒擁有不同的基因型,為了保證單抗制劑對不同病毒株或病毒的不同基因型的有效性,開發“雞尾酒療法”從而針對病毒不同抗原位點勢在必行。WHO也建議抗狂犬病單克隆抗體制劑應將針對病毒不同抗原位點的多株單抗組合成“雞尾酒式”組合制劑[6]。
雙特異性抗體——狂犬病被動免疫新選擇
目前抗體“雞尾酒療法”在臨床運用已非常多見,不過這種組合形式也有一定的缺點,由于需要分別制備不同的單抗然后進行混合,可能在生產過程中影響產品質量。而雙特異性抗體則不存在這一問題,因為其生產工藝與單一單抗類似,因此能夠避免組合制劑生產過程的工藝復雜性,使得質量更加可控,安全性更高。
以智翔金泰自主研發的重組全人源雙特異性抗體GR1801為例,其可同時特異性結合狂犬病毒G蛋白上表位I和III位點,通過阻斷G蛋白與受體的結合,在狂犬疫苗主動免疫完全發揮保護作用前阻滯病毒對神經的侵染,預防狂犬病。
對于中和抗體來說,所面臨的最大問題就是對抗病毒“免疫逃逸”的能力。而雙特異性抗體剛好可以有效針對這一難題。
臨床前數據表明,雙特異性抗體GR1801可有效預防狂犬病毒的免疫逃逸。在對3個狂犬病病毒進化群中的多種狂犬病病毒株的中和試驗中,GR1801對試驗用所有毒株均具有中和作用。體內試驗表明,適當劑量GR1801與致死量病毒中和后,小鼠發病時間明顯延后,以14d(疫苗起效達到保護效果的時間)為觀察終點時,可實現100%保護。比格犬攻毒保護試驗結果表明,0.02mg/kg與狂犬病疫苗聯用已經可以對攻毒比格犬產生100%保護,與HRIG和疫苗聯用組相當。
在中國健康受試者中單次肌肉注射GR1801注射液臨床結果顯示,GR1801免疫原性低、安全性和耐受性均良好。GR1801單藥0.05mg/kg劑量下在起效時間、抗體滴度水平、陽性率、達峰時間上與陽性對照藥物HRIG相當。GR1801目前已進入III期臨床階段,未來將會有更多的臨床數據證明其在狂犬病被動免疫的安全性和有效性。
智翔金泰將抗感染作為主要研發方向,除了狂犬病中和抗體之外,還有一款預防破傷風的單克隆抗體GR2001。破傷風是由破傷風梭菌引起的急性感染性、中毒性疾病,在無醫療干預的情況下,尤其是老年人和嬰幼兒,病死率接近100%。即使經過積極的綜合治療,該病的病死率在全球范圍仍為30-50%。由此可見,GR2001未來潛力也十分值得期待。
總結
狂犬病毒與人類共存了幾千年,如今已經成為了一種可預防的疾病,但是人類與其抗爭的腳步并沒有停止,我們不能掉以輕心,更不能存在僥幸心理。
雙特異性抗體作為被動免疫新的新選擇,不僅能夠提供更高的安全性,也能針對多種狂犬病毒菌株展現中和能力,產生與HRIG相當的保護作用,為狂犬病預防提供了新的“隱形”保護屏障。隨著更多安全性和有效性數據的出爐,相信,這一創新療法的出現將助力減少狂犬病暴露這一目標。
[1]賽諾菲中國官網. https://www.sanofi.cn/zh/high-quality-products/vaccine/vaccine-history
[2] 俞永新. 狂犬病和狂犬病疫苗(第二版)[M]. 北京: 中國醫藥科技出版社; 2009
[3] 狂犬病預防控制技術指南(2016 版). 中國疾病預防控制中心
[4] 《抗狂犬病毒單克隆抗體新藥臨床試驗技術指導原則》起草說明
[5] REGENERON’S CASIRIVIMAB AND IMDEVIMAB ANTIBODY COCKTAIL FOR COVID-19 IS FIRST COMBINATION THERAPY TO RECEIVE FDA EMERGENCY USE AUTHORIZATION. https://newsroom.regeneron.com/news-releases/news-release-details/regenerons-regen-cov2-first-antibody-cocktail-covid-19-receive
[6] WHO consultation on a rabies monoclonal antibody cocktail for rabies post exposure treatment. Geneva, WHO, 23–24 May 2002. Geneva: World Health Organization; 2002.
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容