銀屑病是一種廣泛流行的自身免疫性疾病,影響全球至少6000萬人口[1],僅中國就有超過650萬人患病[2]。由于進展緩慢,絕大部分患者需長期治療,甚至終身用藥,因此銀屑病也會被稱為“不死的癌癥”。為促進世界對銀屑病及患者的關注和正確認識,呼吁人們給予銀屑病患者應有的重視和尊重。自2004年起,每年的10月29日被確立為“世界銀屑病日”(World Psoriasis Day,WPD)。今年,世界銀屑病日的主題為“United we tackle Mental Health,我們攜手并肩,改善心理健康”。目的是號召全社會齊心協力,打破狹隘的“美丑”標準,停止污名化,重視銀屑病患者心理疾病的預防和診斷,為所有銀屑病患者共筑健康和幸福的未來。
來源:IFPA官網
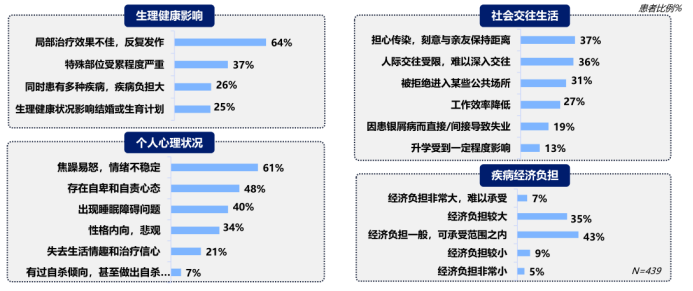
今年銀屑病日主題之所以被定為“改善心理健康”,是因為銀屑病并不只是皮膚病,它還是一種系統性疾病。越來越多的研究表明:銀屑病患者普遍伴有焦慮、睡眠障礙、抑郁癥、社交障礙,甚至自殺傾向。在全球范圍內,每10名銀屑病患者中就有1人被診斷為抑郁癥,每5人就有4人經歷過侮辱和歧視。2018年發布的《中國銀屑病疾病負擔和患者生存質量調研項目研究報告》顯示,銀屑病還是一種社交障礙性疾病,在過去一年有近89%的患者表示有精神壓力,78%的患者遭受過歧視;更令人觸目驚心的是,34%的患者因患銀屑病有自殺念頭,5%的患者曾實施過自殺行為[3]。另一項針對中國銀屑病患者的調查問卷結果顯示,近1/3的患者被拒絕進入某些公共場所,有近19%的患者因銀屑病而直接/間接失業[4]。
以上種種數據都表明,銀屑病不僅對患者個人的生理、心理都會造成嚴重傷害,同時還因為患者群體龐大而產生了巨大的家庭照護和國家公共衛生負擔。因此,銀屑病的臨床治療對于新型的治療藥物或手段一直存在迫切的需求。
銀屑病治療手段持續升級換代
銀屑病根據體表受累面積、銀屑病皮損面積和嚴重程度可以分為輕度、中度和重度,對應的患者比例分別大約為40%,40%和20%。銀屑病的嚴重程度不同,治療方法也不一樣。輕度銀屑病一般皮損累及體表面積<3%,以外用藥物治療為主;中度銀屑病一般皮損累及體表3%-10%之間,在外用藥的基礎上,加用紫外線療法或口服維甲酸或免疫抑制劑。重度銀屑病皮損累及體表面積>10%,或伴發關節受累、呈膿皰型或紅皮病型,此時的主要治療是系統應用免疫抑制劑(如甲氨蝶呤、硫唑嘌呤等、環孢素)、維甲酸或糖皮質激素。不過,這些傳統的治療方式難以取得良好穩定的療效。我國近62%以上的患者對銀屑病治療結果不滿意。一是因為藥物的效果弱、毒性大、副作用多,患者無法耐受,二是因為部分藥物容易致畸,難以達到患者預期的治療效果。隨著疾病機制研究的深入以及業界對銀屑病臨床需求的重視和研發資源投入,銀屑病治療手段一直在升級迭代。特異性更強、療效和安全性更優的藥物持續出現。比如IL-17抑制劑,IL-12/23抑制劑,口服的TYK抑制劑,極大的滿足了臨床患者對創新療法的需求,也驅動了市場的快速增長。據IQVIA Forecast Link預測,2020年到2029年,全球銀屑病藥物市場規模將以年復合增長率(CAGR)3%的增速達到335億美元[5]。尤其是IL-17抑制劑自上市以來,銷售收入實現快速增長,諾華Cosentyx(司庫奇尤單抗)2021年全球銷售額達到47.18億美元,禮來Taltz (ixekizumab)自2018年上市以來,短短4年后也成長為年銷售額22億美元的重磅炸彈。2019年4月,Cosentyx在中國獲批上市,2020和2021年中國銷售額分別達到5億元和15億元。以Cosentyx 4.04萬元的年治療費用計算,2021年約3萬多名患者足療程接受治療,其市場滲透率不足1%。這說明中國銀屑病市場仍存在較大未被滿足的臨床需求。
IL-17革新中重度銀屑病治療格局
白細胞介素17A(IL-17A,又稱IL-17)是重要的促炎因子,在銀屑病這類自身免疫性疾病患者體內大量表達。IL-17A通過與IL-17RA(IL-17A受體)結合,誘導白細胞介素-6(IL-6)、趨化因子CXCL1等下游細胞因子或趨化因子的釋放,繼而誘發炎癥產生或放大炎性癥狀。研究表明,抑制IL-17可阻斷下游信號的傳遞,從而間接抑制炎癥因子的釋放,起到疾病治療作用。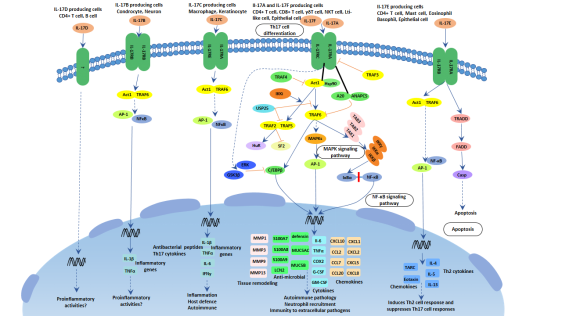
IL-17通路(來源:Cusabio)
IL-17單抗的靶標特異性強,在臨床試驗中也顯示出對銀屑病出色的治療效果。國外一項名為UNCOVER-J的研究中,研究機構對使用依奇珠單抗的患者進行了跟蹤走訪,該研究數據顯示,在使用依奇珠單抗注射液治療16周后,97%的患者實現PASI 75(皮損面積和嚴重程度緩解75%以上),87%的患者實現了PASI 90,40%的患者實現了PASI 100。使用依奇珠單抗注射液治療1周即可實現皮損和瘙癢癥狀顯著改善;治療60周時,55%的患者達到PASI 100,持續用藥,皮損清除效果可穩定維持至少4年[6]。過去近30年,銀屑病治療以皮損面積和嚴重程度緩解(PASI)作為療效評估的“金標準”,指數越高,說明療效越明顯。傳統系統治療藥物的療效目標以PASI 50、PASI 75居多,隨著IL-17等新型生物制劑的問世,銀屑病的治療目標也在不斷刷新。2017意大利中重度銀屑病的系統性治療指南提出,對于重癥患者,應追求PASI 90或更大程度的改善[7]。而《英國皮膚科醫師協會(BAD)銀屑病生物制劑治療指南》、《法國系統治療中重度銀屑病治療指南》等各大權威指南均提出了更高的治療目標PASI 100,即所有的皮損都清除[8,9]。目前IL-17A抑制劑的療效已在銀屑病領域得到廣泛臨床驗證,并成為了指南推薦中重度銀屑病患者的一線治療選擇[7]。總之,自以IL-17為代表的新療法批準治療銀屑病以來,患者的臨床獲益和生活質量均有了顯著提高。尤其是2019年以來,多款IL-17抑制劑在中國上市,這為中國中重度斑塊型銀屑病患者實現皮損清除達到90%(PASI 90)的目標帶來革命性的變化。
國產IL-17新藥即將入局, 進一步提高藥物可及性
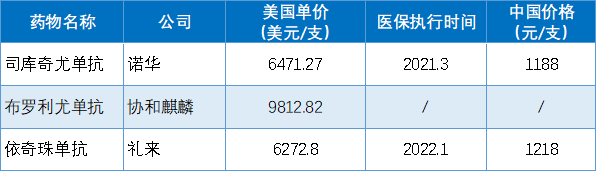
近兩年,國內批準了多款TNF-α抑制劑類生物類似藥,如英夫利西單抗和阿達木單抗,提高了銀屑病患者的藥物可及性,不過這類產品在療效方面遠不及IL-17類藥物[10-12]。目前國內獲批上市的IL-17類創新型銀屑病藥物來自外資藥企,雖然進口產品逐漸被納入醫保目錄,價格大幅壓縮,但是患者的經濟負擔也還是較重。以司庫奇尤單抗為例,其為醫保乙類藥品,年治療費用約為4.04萬元,假設醫保報銷70-80%,患者仍需承擔0.81-1.21萬元/年。國內已獲批上市的IL-17類生物制劑
注:美國單價來源見參考資料[13]
在這樣的情況下,國產的銀屑病創新生物制劑值得期待。一方面,進口產品后續價格下降空間較小,需要國產生物制劑的出現來打破目前的價格平衡,使價格進一步下沉,共同惠及基層患者群體。另一方面,在技術、資本、政策等利好推動下,中國生物醫藥產業已經進入迅速發展期。據估計,到2025年,中國單抗市場規模將達到1810億元,5年復合增長率為34.58%。這意味著國產生物制劑將與進口產品同臺競技,共同搶占巨大市場機會。基于未滿足的臨床需求和巨大市場前景,多家國內企業確實在致力于開發具有自主知識產權的國產銀屑病新藥。由醫藥魔方數據庫可知,開發IL-17、IL-23、IL-36單抗的國產企業包括智翔金泰、恒瑞、信達、君實、康方生物等。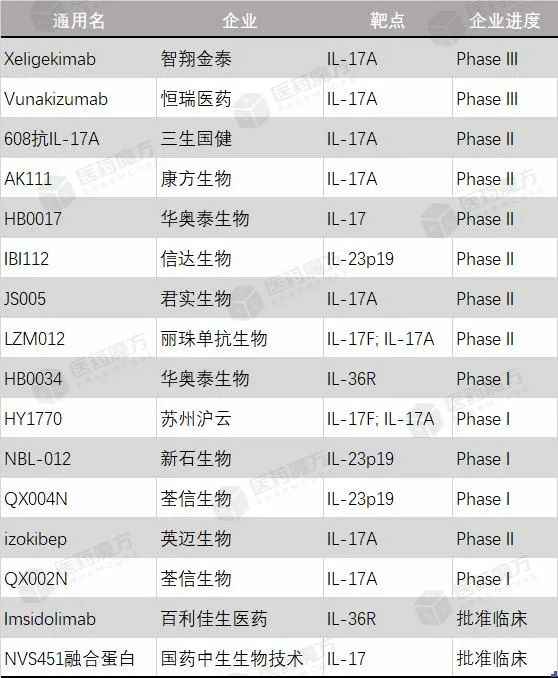
在IL-17賽道,目前尚無國產新藥獲批上市,從開發進度來看,智翔金泰自主研發的Xeligekimab(賽立奇單抗,GR1501)和恒瑞醫藥的Vunakizumab均已進入III期階段,二者有望成為首批上市的國產IL-17A單抗產品,為國內銀屑病患者帶來更多的治療選擇。
總結
IL-17從首次被發現到首個靶向藥獲批上市并成長為重磅炸彈用了30年時間。這也給銀屑病等自免疾病患者帶來了更好的治療手段和選擇。如今這類藥物已經成為中重度銀屑病患者的重要系統性治療藥物之一。不過,對于我國患者而言,進口產品價格高昂,基層滲透率低,治療需求遠未得到滿足。期待國產新藥的上市,惠及更多國內患者。[1] International Federation of Psoriasis Associations (IFPA) World Psoriasis Day website. https://ifpa-pso.com/Last accessed October 2022.
[2] 丁曉嵐等,中國六省市銀屑病流行病學調查,2010,中國皮膚性病學雜志
[3] 北京大學醫藥管理國際研究中心,《中國銀屑病疾病負擔和患者生存質量調研項目研究報告》
[4] 后疫情時代:中國首個銀屑病患者治療現狀及生活質量洞察-調研報告
[5] 全球銀屑病藥物市場概覽和展望:白介素(IL)抑制劑將繼續驅動銀屑病藥物市場增長(IQVIA艾昆緯公眾號)
[6] 禮來銀屑病生物藥依奇珠單抗中國上市,北京、上海已供貨(醫藥魔方info)
[7] P. Gisondi, G. Altomare, F. Ayala, et al. Italian guidelines on the systemic treatments of moderate-to-severe plaque psoriasis. JEADV 2017 DOI: 10.1111/jdv.14114
[8] F. Amatore, A.-P. Villani, M. Tauber, et al. French guidelines on the use of systemic treatments for moderate-to-severe psoriasis in adults. JEADV, 2019 DOI: 10.1111/jdv.15340
[9] Smith CH, Yiu ZZN, Bale T, et al. British Association of Dermatologists guidelines for biologic therapy for psoriasis 2020: a rapid update[J]. Br J Dermatol,2020,183(4): 628-637.
[10] Langley RG, Elewski BE, Lebwohl M, Reich K, Griffiths CE, Papp K, et al. Secukinumab in plaque psoriasis–results of two phase 3 trials. N Engl J Med. 2014;371(4):326–38.
[11] Secukinumab EMEA SUMMARY OF PRODUCT CHARACTERISTICS.
[12] 依奇珠單抗注射液申請上市技術審評報告,中國 CDE,2022 年 6 月
[13] https://www.goodrx.com/healthcare-access/drug-cost-and-savings/most-expensive-drugs-period
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容