
2022-10-20 11:59:28來源:藥智頭條/憶瀏覽量:427
導讀:誰將是“王者”,拭目以待!
FGFR,即成纖維細胞生長因子受體,是目前“不限癌種”療法聚焦的熱門靶點之一;是酪氨酸激酶受體家族中重要的一員,由四種高度保守的跨膜受體酪氨酸激酶(FGFR1~4)和一種能夠結合成FGF配體但缺乏細胞內(nèi)激酶結構域的受體FGFR5(也稱為FGFRL1)組成。
正常生理條件下,F(xiàn)GFR與其配體成纖維細胞生長因子(FGF)結合,F(xiàn)GFR發(fā)生二聚體化以及自身磷酸化,激活下游信號通路,如JAK/STAT通路、磷脂酶C通路,這些信號傳導途徑在多種生理過程如細胞增殖、分化、遷移和凋亡中均起著至關重要的作用。
不過,F(xiàn)GFR容易受各種體細胞畸變的影響,發(fā)生過表達、點突變、基因易位等常見突變,從而導致癌變。研究發(fā)現(xiàn),F(xiàn)GFR基因變異通常在肺癌、肝癌、肝內(nèi)膽管癌、乳腺癌、胃癌、子宮癌及膀胱癌等實體瘤中廣泛存在,而且不同癌種的FGFR突變類型及頻率也存在差異。
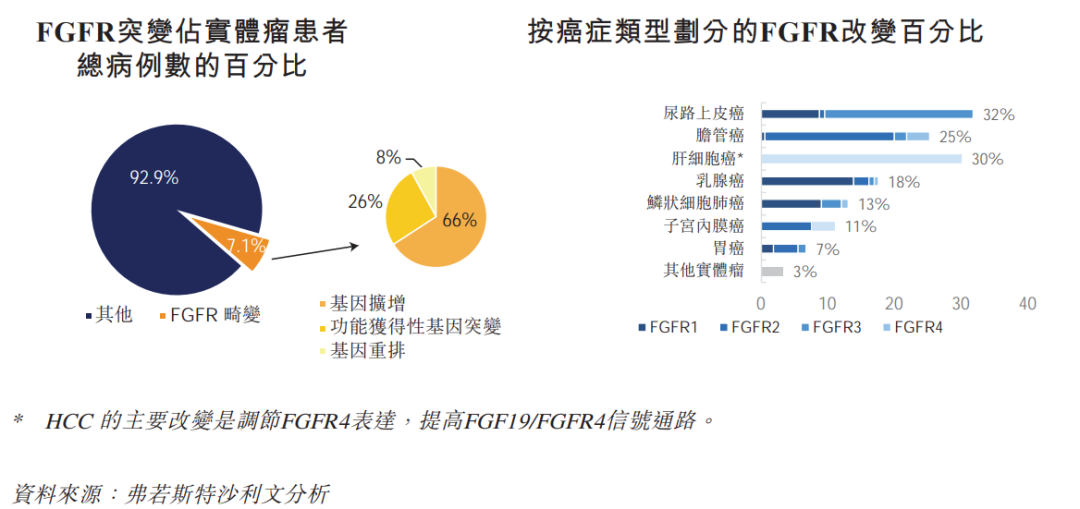
圖片來源:弗若斯特沙利文
2016年美國《ClinicalCancerResearch》雜志發(fā)表的一項涉及4853例實體瘤患者的基因測序分析數(shù)據(jù)顯示:FGFR變異可見于7.1%(360/4853)的腫瘤樣本中,其中66%為基因擴增、26%為基因突變,8%為染色體重排。FGFR1變異率遠高于其它3種亞型,占49%,F(xiàn)GFR2變異率為19%,F(xiàn)GFR3和FGFR4分別占26和7%,并且約有5%患者存在1種以上FGFR亞型變異。
4款已獲批,潛力市場引合作不斷
FGFR抑制劑通過阻斷FGFR介導的信號通路,可以達到抑制腫瘤生長。近年來,F(xiàn)GFR抑制劑進入收獲期,2019年之后每年批準一款,截至目前全球已經(jīng)批準4款,其中僅Pemazyre在國內(nèi)獲批,詳見下表。
全球已批準的FGFR抑制劑

資料來源:公開資料
已獲批的這四款FGFR抑制劑的用藥頻率均為每日口服一次,適應癥主要集中在膽管癌領域。據(jù)悉,這四款FGFR抑制劑均未進入重磅產(chǎn)品行列。不過,Pemazyre2020年、2021年銷售額分別為25.9百萬美元、68.5百萬美元。
且業(yè)界非常看好FGFR抑制劑,NatureReviewDrugDiscovery預計Balversa2024年銷售額有望達到12億美元,EVP預測Truseltiq2026年銷售額可達2.53億美元。
不過,F(xiàn)GFR作為下一個“不限癌種”新靶標,相關抑制劑價格不言而喻—高昂。
據(jù)悉,Balversa的定價為10080美元-22680美元/療程,為期28天。Pemazyre的上市價格為每療程1.7萬美元,平均治療時間約為6個月,8或9個療程,每位患者的成本約為13.6萬至15.3萬美元。Truseltiq價格為每月2.15萬美元,每6個月的價格約為12.9萬美元。昂貴的治療費用價格使得普通患者“望而卻步”,只能遠觀。
不過,作為潛力股,及被業(yè)界看好的市場前景;各大藥企紛紛入局,合作開發(fā)FGFR抑制劑。如:Balversa由Astex公司發(fā)現(xiàn),2008年強生與Astex公司就該藥達成獨家全球授權和合作協(xié)議。
Pemazyre由Incyte公司研發(fā),2018年信達生物與Incyte公司達成合作,獲得包括該藥在內(nèi)的3款藥物單藥或聯(lián)合治療在中國內(nèi)地及香港、澳門和臺灣地區(qū)的臨床開發(fā)與商業(yè)化授權。
Truseltiq是BridgeBio于2018年從諾華Novartis引進,BridgeBio和Helsinn共同負責該藥在美國市場的商業(yè)化,Helsinn負責該藥在美國以外(不包括大中華區(qū))地區(qū)的獨家商業(yè)化。2020年,聯(lián)拓生物與BridgeBio建立戰(zhàn)略聯(lián)盟,負責該藥在大中華區(qū)(中國大陸、香港、澳門)的臨床開發(fā)、注冊申請和未來的商業(yè)運營中國市場的開發(fā)和商業(yè)化。
多款在研FGFR抑制劑蓄勢待發(fā)
目前全球還有多款在研FGFR抑制劑已進入臨床試驗階段,其中拜耳的Rogaratinib和和譽生物/阿斯利康的ABSK091(AZD4547)已進入3期臨床。從下表可以看出,在研FGFR抑制劑的適應癥愈發(fā)豐富,開始涉及非小細胞肺癌、胃癌等實體瘤以及軟骨發(fā)育不全。且FGFR抑制劑的靶點也越來越細化,已有企業(yè)研發(fā)出FGFR3抑制劑、FGFR4抑制劑和FGFR2b抑制劑。此外,F(xiàn)GFR抑制劑的藥物類型也更加豐富,已出現(xiàn)單抗(如:bemarituzumab、Vofatamab)和核素偶聯(lián)藥物(如:FPI-1966)。
全球部分在研FGFR抑制劑
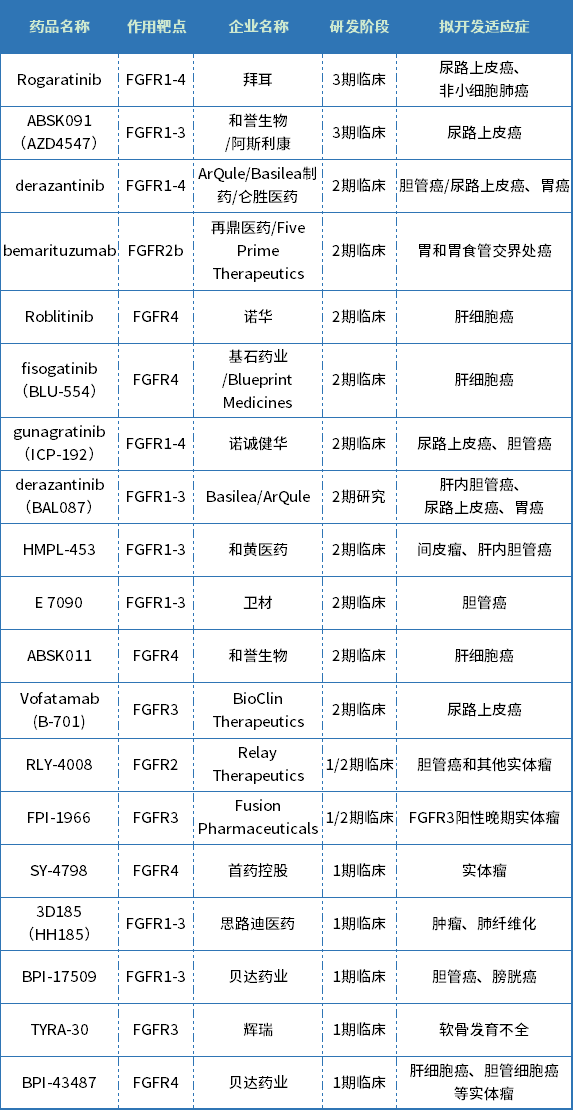
資料來源:公開資料(不完全統(tǒng)計)
值得一提的是,我國藥企也在積極布局FGFR抑制劑市場。且除自主研發(fā),我國藥企還積極從外部引進,如2017年再鼎醫(yī)藥從FivePrime引進bemarituzumab、2018年基石藥業(yè)從BlueprintMedicines引進fisogatinib、2018年侖勝醫(yī)藥從ArQule引進derazantinib、2018年信達生物從Incyte公司引進pemigatinib、2019年和譽生物從阿斯利康引進AZD4547。
總結
公開數(shù)據(jù)顯示,全球FGFR相關實體瘤的總體年發(fā)病人數(shù)已從2016年的440萬人增長到2020年的490萬人,復合年增長率為3.0%,預計到2035年增長至680萬人。
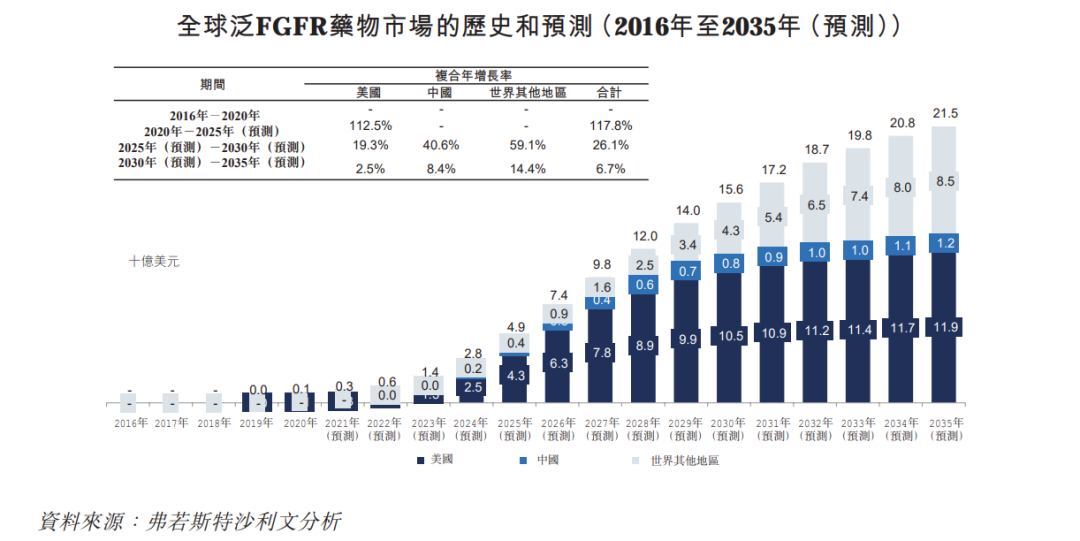
圖片來源:弗若斯特沙利文
隨著患者體量的增加,F(xiàn)GFR抑制劑的市場規(guī)模也將持續(xù)擴張。據(jù)和譽生物招股書,2035年全球泛FGFR抑制劑市場規(guī)模將達到215億美元。但高選擇性FGFR抑制劑目前尚未形成市場規(guī)模。而且,隨著高選擇性FGFR抑制劑的開發(fā),F(xiàn)GFR抑制劑的市場前景更值得期待。
參考資料:
1.和譽生物招股書、企業(yè)公告等公開資料
2.《FGFR抑制劑競爭激烈:3款獲批,多款在研》,亦,貝殼社
聲明:本文系藥方舟轉載內(nèi)容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內(nèi)容、版權和其它問題,請與本網(wǎng)站留言聯(lián)系,我們將在第一時間刪除內(nèi)容