8月22日,石藥集團宣布了兩款在研1類新藥的研發(fā)進展,包括:1)DPP-4抑制劑普盧格列汀片治療2型糖尿病的兩項關鍵3期臨床試驗均達到預設終點,擬于近期在中國遞交上市申請;2)選擇性的NTRK和ROS1雙靶點抑制劑SYHX2009在中國獲批臨床。
DPP-4全稱為二肽基肽酶-4,DPP-4抑制劑是治療糖尿病的主要藥物類型之一。公開資料顯示,這類藥物不僅能夠抑制胰高血糖素樣肽-1(GLP-1)和葡萄糖依賴性促胰島素分泌多肽(GIP)的滅活,提高內(nèi)源性GLP-1和GIP的水平,促進胰島β細胞釋放胰島素,同時還能抑制胰島α細胞分泌胰高血糖素,提高胰島素水平,降低血糖,且不易誘發(fā)低血糖和增加體重。普盧格列汀片(DBPR108片)是石藥集團附屬公司石藥集團中奇制藥的1類新藥,為一種新型口服DPP-4抑制劑,對DPP-4具有高選擇性和強抑制性。據(jù)石藥集團新聞稿介紹,該藥通過抑制DPP-4,使內(nèi)源性活性GLP-1水平升高,從而增強β細胞和α細胞對葡萄糖的敏感性,增加葡萄糖刺激的胰島素分泌并增強葡萄糖對胰升糖素分泌的抑制作用,進而降低血糖水平。石藥集團在中國開展了兩項3期臨床試驗作為DBPR108片治療2型糖尿病的關鍵臨床試驗,用于支持上市申報,分別為DBPR108片單藥3期試驗、DBPR108片聯(lián)合二甲雙胍3期試驗。兩項3期試驗共入組約1000例2型糖尿病受試者,試驗結果均顯示較好的臨床效果,達到預設終點。其中單藥試驗結果顯示,在主要療效終點第24周末糖化血紅蛋白(HbA1c)較基線變化,DBPR108 片組顯著優(yōu)于安慰劑組,同時非劣于陽性藥磷酸西格列汀片組。聯(lián)合試驗結果顯示,在主要療效終點第24周末HbA1c較基線變化, DBPR108片組顯著優(yōu)于安慰劑組。此外,DBPR108片組的安全性數(shù)據(jù)顯示安全性與西格列汀組和安慰劑組相似。石藥集團新聞稿表示,基于以上研究結果擬于近期向中國國家藥品監(jiān)督管理局(NMPA)提交上市前溝通交流的申請。
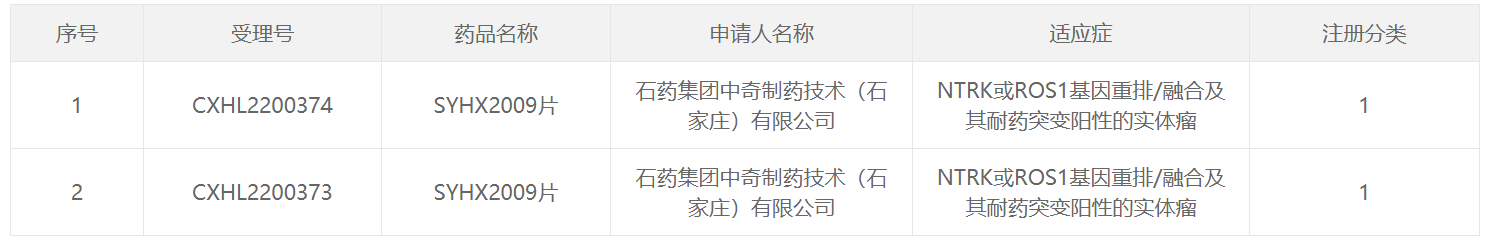
截圖來源:中國國家藥監(jiān)局藥品審評中心(CDE)官網(wǎng)
NTRK中文全稱是神經(jīng)營養(yǎng)因子受體酪氨酸激酶。NTRK融合陽性腫瘤產(chǎn)生的原因是NTRK1/2/3基因與其它基因融合,導致編碼的TRK蛋白出現(xiàn)異常。變異的TRK或者TRK融合蛋白持續(xù)激活,從而引發(fā)永久的信號級聯(lián)反應,這些蛋白在TRK融合癌患者中是驅(qū)動腫瘤增長和轉(zhuǎn)移的主要因素。研究發(fā)現(xiàn),NTRK基因融合可能出現(xiàn)在起源于身體不同位置的腫瘤中,這使得它成為了研究人員開發(fā)“不限癌種”療法的靶標之一。ROS1是一種編碼受體酪氨酸激酶的基因,與間變性淋巴瘤激酶(ALK)結構相似,是非小細胞肺癌明確的一種少見驅(qū)動基因。融合(重排)是ROS1基因的主要變異類型。SYHX2009為石藥集團開發(fā)的1類新藥,為一種選擇性的NTRK和ROS1雙靶點抑制劑。臨床前研究顯示,該產(chǎn)品具有優(yōu)異的體內(nèi)外活性和良好的安全性。本次,該藥獲批臨床的適應癥為:NTRK或ROS1基因重排/融合及其耐藥突變陽性的實體瘤。
聲明:本文系藥方舟轉(zhuǎn)載內(nèi)容,版權歸原作者所有,轉(zhuǎn)載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內(nèi)容、版權和其它問題,請與本網(wǎng)站留言聯(lián)系,我們將在第一時間刪除內(nèi)容!


