
2022-07-22 16:38:58來源:藥方舟瀏覽量:275
7月20日,PTC宣布,歐盟委員會(EC)批準Upstaza(eladocagene exuparvovec)上市,用于治療18個月及以上芳香族L-氨基酸脫羧酶(ADCC)缺乏癥患者。Upstaza不僅是全球首個獲批治療ADCC缺乏癥的疾病修飾療法,還是首個直接注入大腦的基因療法。

AADC缺乏癥是一種罕見的遺傳性神經系統疾病,由編碼ADCC酶的多巴脫羧酶(DDC)基因變異引起。ADCC酶的缺乏會導致多巴胺和血清素無法被合成,而多巴胺的缺乏會導致患者出現運動障礙,包括運動功能減退、肌張力障礙等。遭遇該基因缺乏的兒童,將面臨發育遲緩(尤其是運動機能)、生命縮短等問題,也會出現癲癇樣眼科發作、頻繁嘔吐、睡眠困難等癥狀。
Upstaza是一種基于重組腺相關病毒血清型 2 (AAV2) 的一次性基因替代療法,該重組載體含有功能正常的人類DDC基因。DDC基因可以傳遞合成AADC的指令。通過將重組質粒直接導入至大腦殼核,糾正潛在的遺傳缺陷,提高AADC水平并恢復多巴胺的合成。
Upstaza的療效和安全性已在臨床試驗和同情使用項目中得到了證明。3項關于Upstaza長期隨訪的合并試驗結果(同情用藥, I/II期, IIb期) 已于2021年發表在Molecular Therapy雜志上。
臨床研究期間,對于沒有達到任何發育運動里程碑的患者,在治療3個月后就表現出具有臨床意義的運動技能的改善,該轉變一直持續到治療后的10年。臨床研究中,PDMS-2和AIMS用來評估兒童運動能力,CDIIT和Bayley-III用來評估認知能力和語言能力。Upstaza治療后,患者的各項評分較基線都迅速增加。
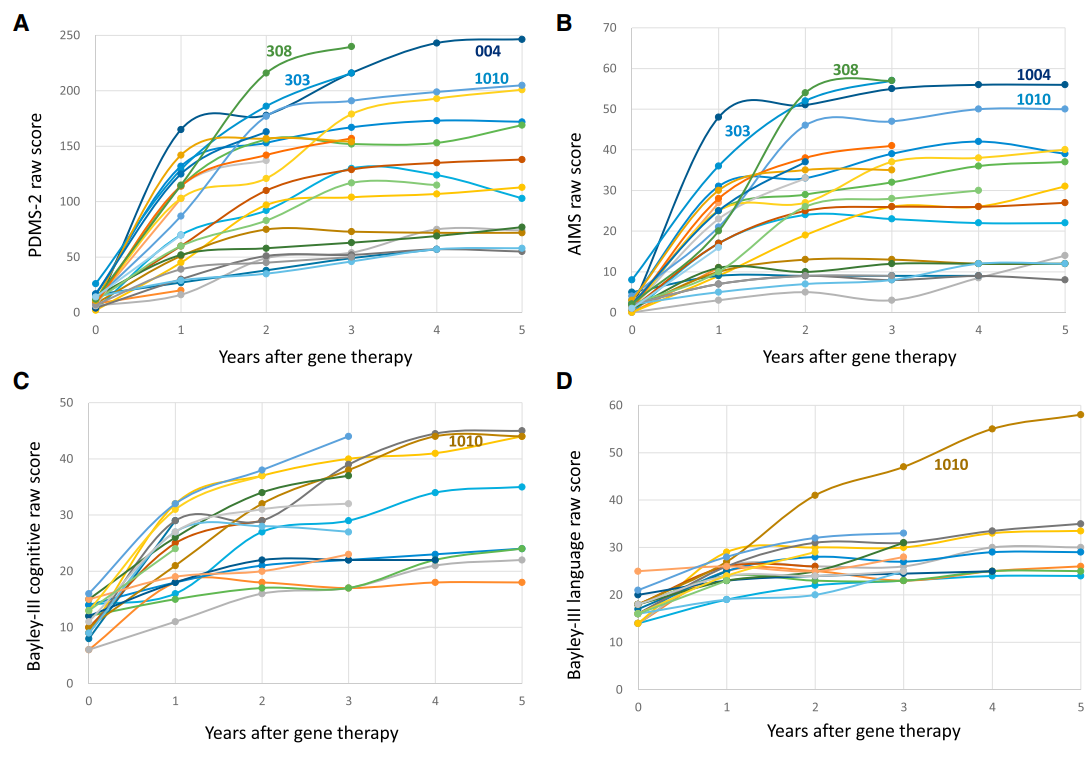
來源:參考資料
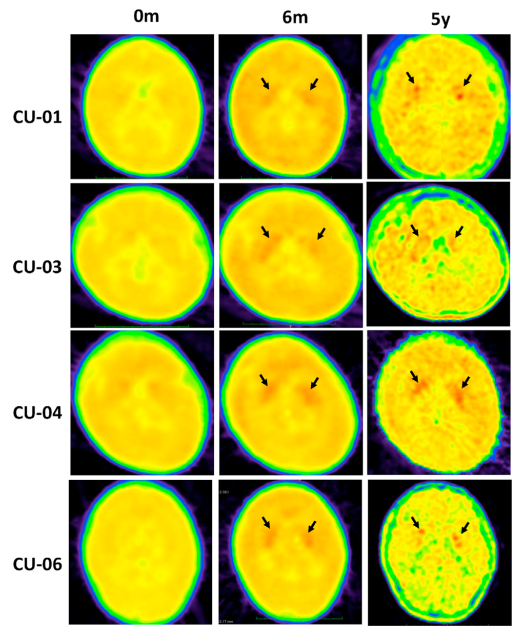
正電子發射斷層掃描(PET)反映了殼核內ADCC活性,Upstaza治療5年后,患者殼核內ADCC活性明顯提高。
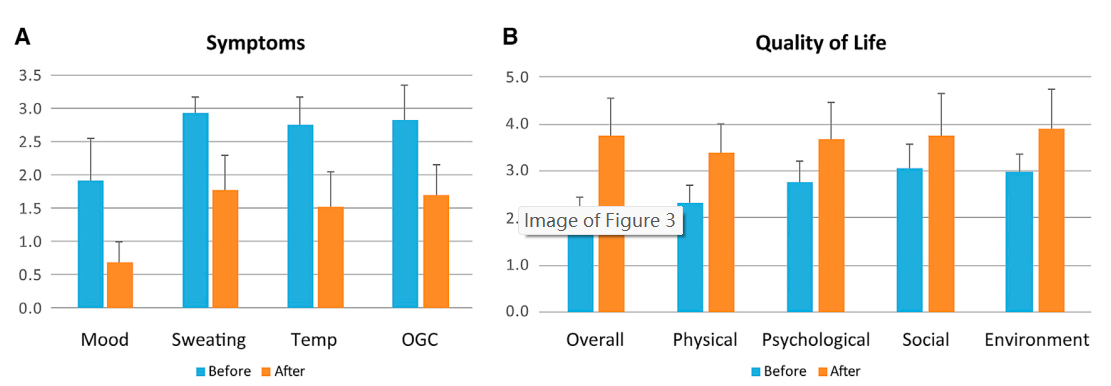
所有接受基因療法治療的患者的嚴重癥狀和生活質量分別得到了緩解和提升。
目前,Upstaza還未在國內申報,期待該藥早日惠及國內的ADCC缺乏癥患者。
參考資料:
[1]Tai CH, et al. Long-term efficacy and safety of eladocagene exuparvovec in patients with AADC deficiency. Mol Ther. 2022;30(2):509-518.
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容!